I. NO - окислитель. Газ лисий хвоствлияние на человека. Диоксид азота: класс опасности :: SYL.ruДиоксид азота – один из самых распространенных загрязнителей атмосферы на сегодняшний день, играющий немалую роль в образовании смога и кислотных осадков. Давайте рассмотрим, что представляет собой это вещество и чем оно опасно для человека. Диоксид азота: формула, характеристикиДвуокись азота – неорганическое соединение состава NO2. Представляет собой газ желто-бурого цвета. В условиях низких температур становится бесцветным. При температуре большей, чем 150°С, происходит диссоциация диоксидана оксид азота и кислород. Данное соединение характеризуется специфическим запахом, который в значительных концентрациях становится удушливым. Имеет высокую химическую активность. Взаимодействует с неметаллами, в реакциях с которыми выступает окислителем. При контакте с водой превращается в азотную кислоту, со щелочной средой – образует нитриты и нитраты. Получение диоксида азота в лабораторных условияхВ лабораториях двуокись азота в основном получают путем воздействия концентрированной азотной кислоты на медь: Cu + 4HNO3 → (CuNO3)2 + 2NO2↑ + 2h3O. Кроме того, соединение образуется при термическом разложении нитрата свинца. В промышленных условиях применяется при производстве азотной и серной кислот, в качестве нитрующего агента для получения безводных нитратов и в роли окислителя в смесевых взрывчатых веществах и жидком ракетном топливе. Антропогенные источники выбросов диоксида азотаБолее 90% от общего количества выбросов оксидов азота попадают в воздушную среду при сжигании различных видов топлива. Начальной формой является NO, который, находясь в воздухе, окисляется кислородом при высокой температуре до NO2. Основные источники, влияющие на выброс диоксида азота в атмосферу:
Бурый оттенок газа позволяет наблюдать его визуально в воздухе больших городов, где суточная динамика концентраций оксидов азота довольно тесно связана с интенсивностью движения автотранспортных средств и солнечного излучения. В утренние часы увеличение количества автомобилей на дорогах приводит к заметному повышению содержания монооксида азота, который с восходом солнца в результате фотохимического окисления переходит в NO2. Также бурый цвет имеют выбросы некоторых химических предприятий, из-за чего их называют «лисьими хвостами». Особенно заметны они летом. Санитарно-гигиенические характеристикиСреди всех окислов группы NOx самым опасным для окружающей среды и человека является именно диоксид азота. Класс опасности – второй. Это значит, что NO2 относится к высокоопасным веществам. Предельно допустимая максимально-разовая концентрация (ПДК) диоксида азота в воздухе населенных пунктов равна 0,085 мг/м3, среднесуточная – 0,04. Для воздуха рабочей зоны установлены другие нормативные значения. Так, значение предельно допустимой концентрации (ПДК р. з.) составляет 2 мг/м3 соединения (диоксид азота). Класс опасности – третий. То есть NO2 отнесен к опасным веществам. Диоксид азота: влияние на человекаВещество характеризуется высокой токсичностью. Диоксид азота в воздухе, даже находясь в относительно небольших концентрациях, способен приводить к существенным изменениям в организме человека. Является острым раздражителем, а также характеризуется общетоксическим действием. Воздействует в основном на органы дыхательной системы. В зависимости от концентраций наблюдаются различные последствия - от слабого раздражения слизистых оболочек глаз и носа до отека легких. Также может приводить к изменениям состава крови, в частности, способствует уменьшению содержания гемоглобина. Ниже рассмотрим подробнее некоторые из эффектов, которые способен вызывать у человека диоксид азота. Влияние на обоняниеДаже если концентрация диоксида азота будет невысокой, люди способны ощущать его специфический запах. Пороговым значением фиксации газа в воздухе для человека считается 0,23 мг на куб. метр. Но при вдыхании диоксида азота в течение 10 минут теряется способность ощущать его запах, что говорит о негативном воздействии на обоняние, выражающемся в его ослаблении. При этом наблюдаются неприятная сухость в горле и раздражение слизистой, которые проходят при концентрации, превышающей пороговое значение обнаружения в 15 раз. Однако на смену приходят другие, более серьезные симптомы, означающие негативное воздействие двуокиси азота на органы дыхания. Влияние диоксида азота на зрениеОдним из последствий комплексного воздействия на слизистые оболочки является ухудшение способности человека видеть в сумерках. Теряется возможность приспособления к отсутствию света. Пороговая концентрация по изменению световой чувствительности глаза составляет 0,14 мг на куб. метр. Учитывая то, что значение обонятельного восприятия почти в два раза выше, можно говорить о способности газа негативно воздействовать и при этом оставаться незамеченным. Влияние на органы дыханияПри относительно невысоких концентрациях диоксид азота в атмосфере способен нарушать дыхание. Так, уже при содержании его в воздухе 0,056 мг на куб. метр у здорового человека наблюдается повышение сопротивления дыхательных путей. Согласно информации Всемирной Организации Здравоохранения, у людей, страдающих хроническими заболеваниями дыхательной системы, данные симптомы наблюдаются уже при содержании NO2 в воздухе, равном 0,04 мг на куб. метр. Результатом воздействия больших концентраций оксидов азота может быть отек легких. Это объясняется следующим. При попадании в организм и взаимодействии с влагой диоксид и оксид азота образуют азотистую и азотную кислоты, разъедающие стенки альвеол легких. Они, как и кровеносные капилляры, становятся легко проницаемыми. В результате сыворотка крови попадает в полость легких. При вдыхании воздух с жидкостью образуют пену, которая нарушает нормальный газообмен, что приводит к возникновению отека легких. При длительном воздействии окисей азота человек становится более восприимчивым к патогенам, которые вызывают болезни дыхательных путей. Ухудшается сопротивляемость легких к бактериям, расширяются альвеолы, клетки в корешках бронхов, чаще наблюдаются бронхиты, воспаление легких и пр. У людей, страдающих сердечно-сосудистыми заболеваниями и хроническими болезнями дыхательных путей, легче развиваются осложнения в случае возникновения кратковременных респираторных инфекций, поскольку у них больше развита чувствительность к прямым воздействиям такого соединения, как диоксид азота. Влияние на человека: другие последствияАзотистая кислота, образующаяся при взаимодействии с влагой в дыхательных путях, вступает в реакцию со щелочными компонентами тканей, превращаясь в результате в нитриты и нитраты. Воздействие этих веществ вызывает ряд негативных последствий. Так, нитриты, всасываясь в кровь, приводят к угнетению центральной нервной системы, образованию метгемоглобина, гемолизу, билирубинемии, расширяют кровеносные сосуды, снижают артериальное давление и пр. Нитраты же при нахождении в кишечнике способны трансформироваться в канцерогенные вещества - нитрозамины. Согласно ряду литературных источников, воздействие двуокиси азота на организм человека снижает его сопротивляемость к заболеваниям, приводит к кислородному голоданию тканей. Особенно остро это проявляется у детей. Также диоксид азота способствует повышению действия канцерогенных веществ и возникновению в результате этого злокачественных новообразований. Некоторые из исследователей связывают повышенную смертность от раковых и сердечно-сосудистых заболеваний в определенных районах с высоким содержанием NO2 в воздушной среде. Хроническое отравление диоксидом азотаДлительная работа в условиях присутствия диоксида азота в воздухе приводит к развитию хронических заболеваний, наиболее распространенными среди которых являются: трахеит, бронхит, перфорация носовой перегородки, пневмосклероз и др. У людей, которые работали на протяжении 3-5 лет при содержании NO2 в воздухе рабочей зоны 0,8-5 мг на куб. метр, наблюдались хронические бронхиты, воспалительные изменения слизистой оболочки десен, осложненный астмоидными приступами пневмосклероз, бронхоэктазии. Кроме того, отмечались повышения максимальной осмотической резистентности эритроцитов, ускорение свертывания крови, тенденция к гипотонии, гранулоцитоз, снижение активности каталазы, содержания сахара и уровня глобулинов и альбуминов в крови. У детей, проживающих на территориях, где диоксид азота присутствовал в концентрациях 0,117-0,205 мг на куб. метр, выявлены изменения объема форсированного выдоха, повышение заболеваемости. Кроме того, в мазках крови наблюдались изменения в конфигурации лимфоцитов и моноцитов, увеличение резистентности эритроцитов. ВыводыКак видим из вышеприведенного материала, азота диоксид в атмосферном воздухе может крайне негативно сказываться на организме человека. К сожалению, превышения допустимых концентраций этого вещества в воздухе – не редкость. Поэтому довольно актуальными на сегодняшний день являются вопросы, касающиеся разработки мероприятий, направленных на снижение выбросов диоксида азота в атмосферу, которые имеют как экологическое, так и санитарно-гигиеническое значение. www.syl.ru Лисий хвост - MEL ChemistryРеагентыБезопасность
Общие правила безопасности
Информация о первой помощи
Рекомендации для родителей
Часто задаваемые вопросыУ меня нет чистой чашки Петри с синим кружком. Что делать?Если вы использовали чашку Петри с синим кружком в опыте с получением хлора Cl2, просто помойте её и высушите бумажным полотенцем. Другая чашка Петри для этого опыта не подойдёт, т.к. из-за высоты крышечки, помещаемой в центр, она не сможет обеспечить необходимую герметичность. Для чего нужен шаблон?Выберите соответствующий данному опыту шаблон и поставьте на него чашку Петри. Подписи около кружков подскажут, какое вещество было использовано в начале опыта, и вы сможете легко сравнить цвет веществ в баночке и в капле после эксперимента. Спустя указанное время капли не поменяли свой цвет. Почему?Убедитесь, что выиспользуете чашку Петри с синими кружками, и газ не выходит через щели. Также важно хорошо смочить содержимое крышечки гидросульфатом натрия NaHSO4. Раствор тимолового синего имеет жёлтый цвет. Это нормально?Всё в порядке. Раствор тимолового синего может пожелтеть, так как он легко поглощает углекислый газ CO2 из воздуха в баночке. Вы можете использовать и такой раствор тимолового синего в дальнейших экспериментах, но при этом цвет жидкости будет меняться не с синего на жёлтый, а с жёлтого на красный. Если вы хотите получить синий раствор, вылейте в пластиковый стаканчик весь тимоловый синий и добавьте к нему 1 каплю гидроксида натрия NaOH. Раствор станет синим и будет готов к использованию в опыте. Другие экспериментыПошаговая инструкция
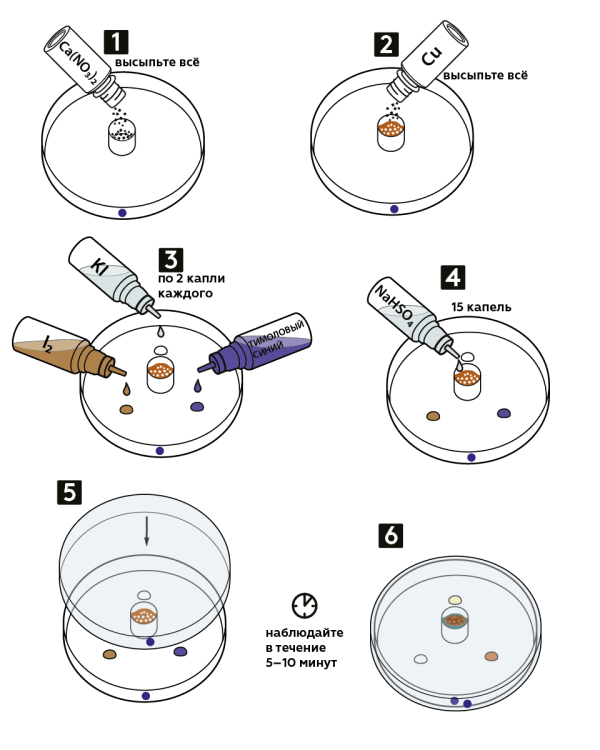 УтилизацияУтилизируйте отходы эксперимента вместе с бытовым мусором. Содержимое пластиковой крышки предварительно разбавьте большим количеством воды. Что произошлоПочему содержимое колпачка синеет?Синюю окраску реакционной смеси придают ионы меди Cu2+. В процессе реакции рыжевато-розовый порошок меди окисляется (отдаёт свои электроны), образуя ионы Cu2+ в составе нитрата меди: Cu + 2Ca(NO3)2 + 4NaHSO4 → Cu(NO3)2 + 2NO2↑ + 2Na2SO4 + 2CaSO4 + 2h3O Именно Cu(NO3)2 придаёт смеси характерный цвет. Узнать больше Вы, наверное, не раз замечали голубовато-зелёные пятна на изделиях из меди и её сплавов. Старинные бронзовые статуи часто полностью покрыты такой «плёнкой». Подобный слой носит название патина и образуется в результате медленного взаимодействия меди с водой, кислородом O2 и углекислым газом CO2 воздуха: 2Cu + CO2 + O2 + h3O → (CuOH)2CO3 Цвет этому соединению также придают ионы меди. Кстати, природный минерал, состоящий из гидроксокарбоната меди (CuOH)2CO3, называется малахит. Помимо этого, ион Cu2+ входит в состав таких ярко окрашенных минералов, как бирюза и азурит. Почему закрытая чашка становится бурой внутри?Если в процессе эксперимента под определённым углом посмотреть на закрытую чашку, то можно заметить, что газ внутри неё имеет бурый цвет. Диоксид азота NO2, который образуется в процессе реакции, описанной в предыдущем вопросе, имеет бурую окраску. Таким образом, появление соответствующего окрашивания внутри чашки – верный признак успешного опыта. Узнать больше Интересно, что диоксид азота приобретает бурую окраску только при сильном нагреве. Уже при температуре ниже 21oС молекулы NO2 начинают попарно объединяться, образуя оксид с формулой N2O4. Образующийся димер бесцветен и существует преимущественно в жидком состоянии. Что произошло с йодидом калия?Резкое изменение цвета раствора и выпадение чёрного осадка произошло из-за окисления иодид-иона (I-) диоксидом азота: 2KI + 2NO2 → 2KNO2 + I2↓ Образовавшийся в результате молекулярный йод в кислой среде не только окрашивает раствор в бурый цвет, но и частично выпадает в осадок. Что произошло с раствором йода?Суть происходящих в данной капле процессов заключается в том же, что и в случае раствора йодида калия KI (см. предыдущий вопрос). Следует помнить, что настойка йода – это раствор йода в растворе йодида калия. Сам по себе йод плохо растворяется в воде, но в присутствии йодида калия образуется вполне устойчивое вещество KI3, чью структуру можно более точно передать как KI*I2. Когда диоксид азота окисляет иодид-анионы, молекулярному йоду становится не с чем связываться, и он также выпадает в осадок. Что произошло с тимоловым синим?Краситель тимоловый синий относится к группе химических веществ, называемых индикаторами. Его раствор меняет цвет в зависимости от того, сколько ионов водорода H+ находится в составе молекулы. Сама молекула индикатора имеет очень сложное строение, поэтому для простоты обозначим её как «Ind». Для тимолового синего характерны три формы: Indh3 ↔ IndH- ↔ Ind2- Каждый вариант придаёт раствору свой цвет: Indh3 – красный, IndH- – жёлтый, Ind2- – синий. Почему же раствор индикатора изменил свой цвет? При растворении диоксида азота в воде образуется смесь азотной (HNO3) и азотистой (HNO2) кислот: 2NO2 + h3O → HNO3 + HNO2 В растворе молекулы этих кислот диссоциируют (распадаются на ионы) с образованием протонов (H+): HNO3 ↔ H+ + (NO3)- HNO2 ↔ H+ + (NO2)- Теперь в растворе присутствуют ионы водорода H+ в количестве, достаточном для перехода части молекул тимолового синего из формы IndH- в форму Indh3. В результате раствор окрашивается в оранжевый цвет. Это интересноСколько у азота оксидов?Азот – уникальный элемент! Для него характерно наличие целого ряда достаточно устойчивых оксидов, практически каждый из которых имеет свою область применения. Давайте с ними познакомимся. Оксид азота (I) N2O Это соединение также носит название «закись азота» или «веселящий газ». Открытое ещё в середине XXI века, это вещество прочно заняло своё место в медицине, технике и пищевой промышленности. Из-за крайне низкой токсичности и быстрого выведения из организма, оксид диазота используют в качестве ингаляционного наркотизирующего вещества. Чаще всего он находит применение в стоматологической практике (когда нет необходимости надолго погружать пациента в сон). Также закись азота используют в качестве наркоза при родах, поскольку он нетоксичен для ребёнка. В пищевой промышленности N2O используется в основном для производства баллонов со взбитыми сливками. Именно он выталкивает содержимое упаковки наружу, образуя аппетитную пышную пену. Закись азота, используемая для медицинских и пищевых нужд, должна быть очень чистой. Если в ней содержится много примесей, такое вещество называется технической закисью азота. Технический газ применяют в качестве компонента топлива. Многие автомобили, участвующие в скоростных заездах, оборудованы специальной системой, которая вводит в двигатель закись азота. Это позволяет повышать эффективность обычного топлива и развивать очень большую скорость. К сожалению, подобное «улучшение» очень плохо влияет на сам двигатель, не рассчитанный на подобные нагрузки. Оксид азота (II) NO NO – газ без цвета и запаха. На воздухе он быстро окисляется до оксида азота (IV), речь о котором пойдёт ниже. Прямого применения в промышленности оксид азота (II) не имеет. Зато это соединение нашло своё место в медицине: его используют в качестве ингаляционной смеси с кислородом для облегчения дыхания у пациентов с заболеваниями лёгких. Окись азота способна расширять сосуды и облегчать поступление кислорода в организм. Также подобные смеси применяют для лучшего раскрытия лёгких у недоношенных детей. Важным открытием в биологии в своё время явилось обнаружение биологической активности молекулы NO – многие процессы в нашем организме не обходятся без её участия. Но, помимо всех преимуществ окиси азота, у неё есть один минус – она способствует разрушению озонового слоя земли. Успокаивает лишь тот факт, что очень малое количество молекул NO может добраться до нужной высоты. Да и не деятельность человека, а грозовые разряды служат основным источником этого вещества в природе. Эти же разряды создают и озон, так что в отношении участия окиси азота в образовании озоновых дыр можно не беспокоиться. Оксид азота (III) N2O3 Самый красивый из оксидов азота. Неустойчивое соединение, легко распадающееся на смесь NO и NO2. Устойчив только при температурах ниже -4oC. Представляет собой синюю жидкость, при более сильном охлаждении (ниже -100oC) становится твёрдым. Из-за своей неустойчивости не имеет промышленного применения. Зато служит для получения в химических лабораториях чистой азотистой кислоты (HNO2) и её солей. Оксид азота (IV) NO2 Этот оксид наиболее широко используется в промышленности. Дело в том, что именно он является сырьём для получения азотной кислоты, речь о которой пойдёт в следующем вопросе. Это бурый газ с резким запахом. При низких температурах образует бесцветные димеры (N2O4). Если вам не повезло и в вашем городе есть промышленное предприятие, из труб которого поднимается рыжевато-бурый дым, то вы имеете возможность наблюдать выброс диоксида азота своими глазами. Такие выбросы получили название «лисий хвост» из-за характерного цвета. К счастью, в настоящее время практически все заводы оснащены системами очистки воздуха, не допускающими попадания NO2 в атмосферу. Это делается для предотвращения «кислотных дождей», губительно действующих на живые организмы. Между прочим, в холодных регионах до того, как были установлены системы очистки дыма, можно было наблюдать димеризацию диоксида азота своими глазами! В сильные морозы (ниже -25oC) «лисьи хвосты» внезапно становились бесцветными. Оксид азота (V) N2O5 Этот оксид представляет собой неустойчивое вещество. Его летучесть и взрывоопасность не позволяют найти ему никакого практического применения, поэтому существует он только в химических лабораториях, причём недолго. Для каждого эксперимента его получают заново и даже не пытаются сохранить про запас. Азотная кислотаГоворя о диоксиде азота, нельзя не упомянуть об азотной кислоте, ведь это важнейший продукт современной химической промышленности! Обратимся к истории. До начала XX века природная натриевая селитра (NaNO3) являлась основным сырьём для производства азотной кислоты, необходимой при изготовлении бездымного пороха. В 1904 году был открыт метод управляемого синтеза окислов азота, который, однако, требовал огромного количества энергии. Так что природные селитры оставались основным источником связанного азота для химической промышленности, а также сельского хозяйства, где они используются в качестве удобрений. Благодаря открытию в 1913 году аммиачного метода связывания атмосферного азота, химическая промышленность смогла отказаться от дефицитного природного сырья. Сейчас вся азотная кислота производится методом растворения диоксида азота в воде в присутствии кислорода: 4NO2 + O2 + 2h3O → 4HNO3 Нитрат натрия, используемый в качестве азотного удобрения, получается при производстве азотной кислоты в процессе поглощения раствором соды остаточных окислов азота: Na2CO3 + NO2 → NaNO3 + NaNO2 + CO2↑ Таким образом, технология получения оксида азота (IV) позволила уменьшить расходы на сельское хозяйство и химическую промышленность. Говоря об азотной кислоте, нельзя также обойти вниманием интересное вещество под названием «царская водка». Оно представляет собой смесь из одного объёма концентрированной азотной кислоты HNO3 и трёх объёмов концентрированной соляной кислоты HCl. Царская водка обладает уникальными свойствами. В ней можно растворить благородные металлы, такие как золото, платина, палладий. Растворение происходит не только посредством окисления металлов кислотами, но и за счёт образования сложных растворимых соединений этих элементов. Не будем подробно рассматривать эти процессы, поскольку химия их сложна для восприятия. Помимо растворения благородных металлов, царская водка используется для получения довольно важного соединения – хлорида олова (IV): 4HCl + 2HNO3 + Sn → SnCl4 + NO2 + NO + 3h3O melscience.com Оксид азота(IV) - это... Что такое Оксид азота(IV)?Бурый газОксид азота (IV) (диоксид азота, бурый газ) NO2 — газ, красно-бурого цвета, с характерным острым запахом или желтоватая жидкость. В обычном состоянии NO2 существует в равновесии со своим димером N2O4. Склонность к его образованию объясняется наличием в молекуле NO2 неспаренного электрона. При температуре 140 °C диоксид азота состоит только из молекул NO2, он очень тёмного, почти чёрного цвета. В точке кипения NO2 представляет собой желтоватую жидкость, содержащую около 0,1 % NO2. При температуре ниже 21°С — это бесцветная жидкость (или желтоватая из-за примеси мономера). При температуре ниже −12 °C белые кристаллы состоят только из молекул N2O4. ПолучениеВ лаборатории NO2 обычно получают воздействием концентрированной азотной кислотой на медь: Также его можно получить термическим разложением нитрата свинца, однако при проведении реакции следует соблюдать осторожность: Химические свойстваКислотный оксид, ему соответствуют азотная и азотистая кислоты. NO2 отличается высокой химической активностью. Он взаимодействует с неметаллами (фосфор, сера и углерод горят в нём). В этих реакциях NO2 — окислитель: Окисляет SO2 в SO3 — на этой реакции основан нитрозный метод получения серной кислоты: При растворении оксида азота(IV) в воде образуются азотная и азотистая кислоты (реакция диспропорционирования): Поскольку азотистая кислота неустойчива, при растворении NO2 в тёплой воде образуются HNO3 и NO: Если растворение проводить в избытке кислорода, образуется только азотная кислота (NO2 проявляет свойства восстановителя): При растворении NO2 в щелочах образуются как нитраты, так и нитриты: Жидкий NO2 применяется для получения безводных нитратов: ПрименениеВ производстве серной и азотной кислот, в качестве окислителя в жидком ракетном топливе и смесевых взрывчатых веществах. Физиологическое действиеОксид азота (IV) высокотоксичен. Даже в небольших концентрациях он раздражает дыхательные пути, в больших концентрациях вызывает отёк лёгких. «Лисий хвост»На фото справа — «лисий хвост» на Нижнетагильском металлургическом комбинате«Лисий хвост» — жаргонное название выбросов в атмосферу оксидов азота на химических предприятиях (иногда — из выхлопных труб автомобилей). Название происходит от оранжево-бурого цвета диоксида азота. При низких температурах диоксид азота димеризуется и становится бесцветным. В летний сезон «лисьи хвосты» наиболее заметны, так как в выбросах возрастает концентрация мономерной формы. Вредное воздействиеОксиды азота, улетучивающиеся в атмосферу, представляют серьёзную опасность для экологической ситуации, так как способны вызывать кислотные дожди, а также сами по себе являются токсичными веществами, вызывающими раздражение слизистых оболочек. Двуокись азота воздействует в основном на дыхательные пути и легкие, а также вызывает изменения состава крови, в частности, уменьшает содержание в крови гемоглобина. В специальной литературе также указывается на то, что воздействие на организм человека диоксида азота снижает сопротивляемость к заболеваниям, вызывает кислородное голодание тканей, особенно у детей. Усиливает действие канцерогенных веществ, способствуя возникновению злокачественных новообразований. Образующаяся в результате взаимодействия диоксида азота с водой азотная кислота является сильным коррозионным агентом. dic.academic.ru Лисий хвост - MEL ChemistryРеагентыБезопасность
Общие правила безопасности
Информация о первой помощи
Рекомендации для родителей
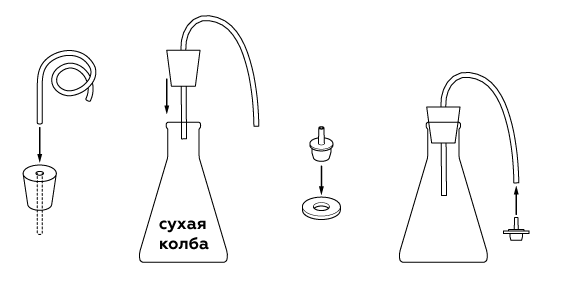
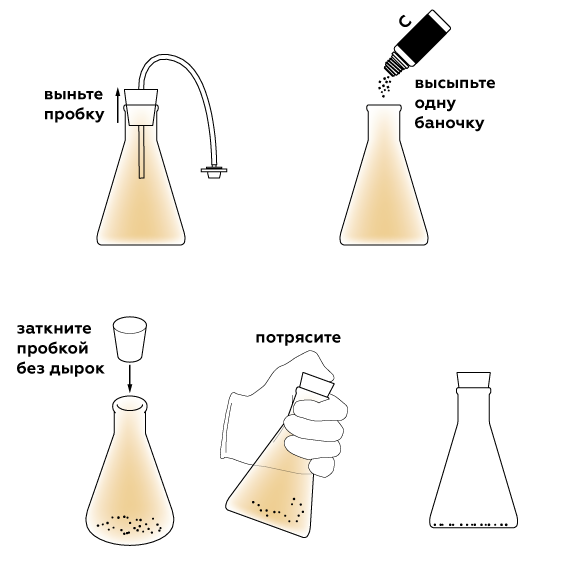
Часто задаваемые вопросыПрошло 10 минут, а колба до сих пор не наполнилась газом. Что не так?Первым делом убедитесь, что вы взяли сухую колбу. Оксид азота(IV) NO2 хорошо растворяется в воде, то есть переходит в воду с образованием азотной и азотистой кислот. Другими словами, во влажной колбе вы могли его просто не заметить. Если с первым пунктом всё хорошо, убедитесь, что вы взяли горячую воду. Для этого осторожно наклейте на стакан термостикер: если он быстро стал желтым, то вода горячая. Если же цвет стикера не изменился, аккуратно вылейте из стакана остывшую воду и налейте горячую до отметки «100 мл». Подождите еще 5–10 минут. Всё еще не работает? Аккуратно откройте баночку и снова перемешайте содержимое палочкой. Затем закройте баночку и опустите ее в горячую воду. Другие экспериментыПошаговая инструкцияПодготовим колбу для сбора газа.
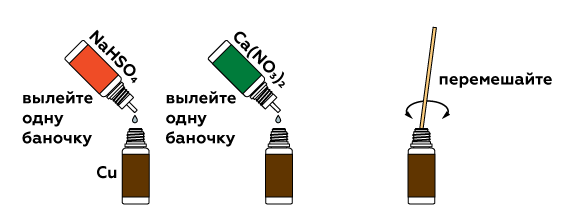
Чтобы получить оксид азота NO2, сначала смешаем нитрат кальция Ca(NO3)2 и гидросульфат натрия NaHSO4. При этом образуется азотная кислота HNO3, которая восстанавливается медью Cu до NO2.
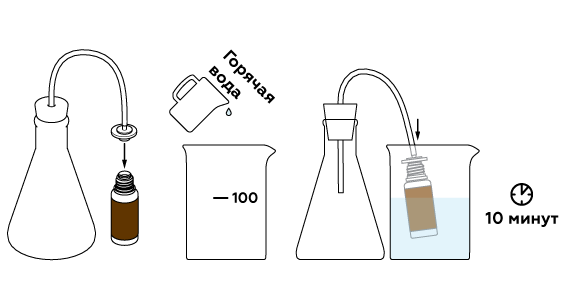
Для ускорения реакции нагреем реакционную смесь.
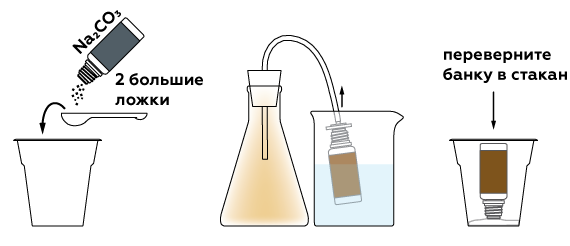
Чтобы остановить реакцию, нейтрализуем кислоту карбонатом натрия.
Рыжий газ в колбе — оксид азота NO2. Этот газ охотно оседает — адсорбируется на активированном угле, который обладает очень большой площадью поверхности. Это позволяет легко поглотить практически весь газ.
Ожидаемый результатДиоксид азота собирается в виде бурого газа, который хорошо поглощается активированным углем. УтилизацияУтилизируйте твердые отходы эксперимента вместе с бытовым мусором. Растворы слейте в раковину и затем тщательно промойте ее водой. Что произошлоКак образуется диоксид азота?Всё начинается, когда мы смешиваем растворы гидросульфата натрия NaHSO4 и нитрата кальция Ca(NO3)2 c медным порошком. Сначала гидросульфат натрия реагирует с нитратом кальция с образованием азотной кислоты: 2NaHSO4 + Ca(NO3)2 → CaSO4 + Na2SO4 + 2HNO3 Узнать больше Эта реакция не так проста, как кажется. Она возможна благодаря одному очень важному химическому явлению – электролитической диссоциации. Как только соль — например, гидросульфат натрия NaHSO4 — попадает в воду, она начинает распадаться (или диссоциировать). Частицы, которые при этом образуются, называются ионами: NaHSO4 → Na+ + HSO42− Ионы могут быть заряжены положительно (например, ион натрия Na+) или отрицательно, как в случае с гидросульфат-ионом HSO42−. Положительно заряженные ионы называют катионами, а отрицательно заряженные — анионами. Затем гидросульфат-анион тоже распадается: HSO42− → H+ + SO42− При этом высвобождается катион водорода (протон) — важная составляющая любой кислоты. Когда в растворе много протонов, химики говорят, что он имеет кислую среду. В растворе гидросульфата натрия содержится много протонов, поэтому добавив к нему нитрат кальция, можно легко получить азотную кислоту. При растворении нитрата кальция тоже образуются ионы: Ca(NO3)2 → Ca2+ + 2NO3− Нитрат-анионы NO3− взаимодействуют с протонами, и образуется азотная кислота HNO3: H+ + NO3− → HNO3. Образовавшаяся азотная кислота реагирует с медью. При этом образуется нитрат меди(II) Cu(NO3)2 и бурый газ — диоксид азота NO2, который и накапливается в колбе.Зачем мы греем реакционную смесь?Повышенная температура заметно ускоряет реакцию. Если бы в нашем эксперименте реакционная смесь не нагревалась, диоксид азота наполнял бы колбу слишком долго. Соответственно, чем теплее смесь, тем быстрее выделяется газ. Как тепло увеличивает скорость реакции? В реакционной смеси содержится бесчисленное количество молекул — маленьких частичек, которые постоянно перемещаются в пространстве. Чаще всего химическая реакция — это процесс, при котором молекула одного вещества сталкивается с молекулой другого вещества, и получается молекула (или молекулы) продукта (или продуктов) реакции. Под воздействием тепла молекулы двигаются быстрее, поэтому вероятность того, что молекулы исходных веществ столкнутся и образуют продукты реакции, становится выше. Правило Вант-Гоффа гласит, что повышение температуры на 10o С ускоряет реакцию в 2–4 раза. Только представьте, насколько ускорилась реакция в нашем эксперименте! Почему нужно нейтрализовать реакционную смесь?Диокисд азота продолжит выделяться и после того, как колба наполнится этим бурым газом. Для нашего эксперимента этого газа достаточно, поэтому реакцию нужно остановить. Луше всего для этого нейтрализовать азотную кислоту, что и делает карбонат натрия Na2CO3. В итоге образуются нитрат натрия NaNO3, вода и углекислый газ CO2: Na2CO3 + 2HNO3 → 2NaNO3 + h3O + CO2↑ Теперь, когда в смеси больше не остается азотной кислоты, реакция прекращается и углекислый газ мгновенно улетает в атмосферу. Пластиковый стаканчик с баночкой можно утилизировать с бытовым мусором. Почему диоксид азота исчезает из колбы?Так происходит из-за выдающихся адсорбционных свойств активированного угля. Когда мы трясем колбу, всё больше молекул диоксида азота попадает в поры активированного угля и уже не может выбраться из них. В результате газ обесцвечивается и кажется, будто бурый диоксид азота исчезает из колбы. Это интересноСколько у азота оксидов?Азот – уникальный элемент! Для него характерно наличие целого ряда достаточно устойчивых оксидов, практически каждый из которых имеет свою область применения. Давайте с ними познакомимся. Оксид азота (I) N2O Это соединение также носит название «закись азота» или «веселящий газ». Открытое ещё в середине XXI века, это вещество прочно заняло своё место в медицине, технике и пищевой промышленности. Из-за крайне низкой токсичности и быстрого выведения из организма, оксид диазота используют в качестве ингаляционного наркотизирующего вещества. Чаще всего он находит применение в стоматологической практике (когда нет необходимости надолго погружать пациента в сон). Также закись азота используют в качестве наркоза при родах, поскольку он нетоксичен для ребёнка. В пищевой промышленности N2O используется в основном для производства баллонов со взбитыми сливками. Именно он выталкивает содержимое упаковки наружу, образуя аппетитную пышную пену. Закись азота, используемая для медицинских и пищевых нужд, должна быть очень чистой. Если в ней содержится много примесей, такое вещество называется технической закисью азота. Технический газ применяют в качестве компонента топлива. Многие автомобили, участвующие в скоростных заездах, оборудованы специальной системой, которая вводит в двигатель закись азота. Это позволяет повышать эффективность обычного топлива и развивать очень большую скорость. К сожалению, подобное «улучшение» очень плохо влияет на сам двигатель, не рассчитанный на подобные нагрузки. Оксид азота (II) NO NO – газ без цвета и запаха. На воздухе он быстро окисляется до оксида азота (IV), речь о котором пойдёт ниже. Прямого применения в промышленности оксид азота (II) не имеет. Зато это соединение нашло своё место в медицине: его используют в качестве ингаляционной смеси с кислородом для облегчения дыхания у пациентов с заболеваниями лёгких. Окись азота способна расширять сосуды и облегчать поступление кислорода в организм. Также подобные смеси применяют для лучшего раскрытия лёгких у недоношенных детей. Важным открытием в биологии в своё время явилось обнаружение биологической активности молекулы NO – многие процессы в нашем организме не обходятся без её участия. Но, помимо всех преимуществ окиси азота, у неё есть один минус – она способствует разрушению озонового слоя земли. Успокаивает лишь тот факт, что очень малое количество молекул NO может добраться до нужной высоты. Да и не деятельность человека, а грозовые разряды служат основным источником этого вещества в природе. Эти же разряды создают и озон, так что в отношении участия окиси азота в образовании озоновых дыр можно не беспокоиться. Оксид азота (III) N2O3 Самый красивый из оксидов азота. Неустойчивое соединение, легко распадающееся на смесь NO и NO2. Устойчив только при температурах ниже -4oC. Представляет собой синюю жидкость, при более сильном охлаждении (ниже -100oC) становится твёрдым. Из-за своей неустойчивости не имеет промышленного применения. Зато служит для получения в химических лабораториях чистой азотистой кислоты (HNO2) и её солей. Оксид азота (IV) NO2 Этот оксид наиболее широко используется в промышленности. Дело в том, что именно он является сырьём для получения азотной кислоты, речь о которой пойдёт в следующем вопросе. Это бурый газ с резким запахом. При низких температурах образует бесцветные димеры (N2O4). Если вам не повезло и в вашем городе есть промышленное предприятие, из труб которого поднимается рыжевато-бурый дым, то вы имеете возможность наблюдать выброс диоксида азота своими глазами. Такие выбросы получили название «лисий хвост» из-за характерного цвета. К счастью, в настоящее время практически все заводы оснащены системами очистки воздуха, не допускающими попадания NO2 в атмосферу. Это делается для предотвращения «кислотных дождей», губительно действующих на живые организмы. Между прочим, в холодных регионах до того, как были установлены системы очистки дыма, можно было наблюдать димеризацию диоксида азота своими глазами! В сильные морозы (ниже -25oC) «лисьи хвосты» внезапно становились бесцветными. Оксид азота (V) N2O5 Этот оксид представляет собой неустойчивое вещество. Его летучесть и взрывоопасность не позволяют найти ему никакого практического применения, поэтому существует он только в химических лабораториях, причём недолго. Для каждого эксперимента его получают заново и даже не пытаются сохранить про запас. Азотная кислотаГоворя о диоксиде азота, нельзя не упомянуть об азотной кислоте, ведь это важнейший продукт современной химической промышленности! Обратимся к истории. До начала XX века природная натриевая селитра (NaNO3) являлась основным сырьём для производства азотной кислоты, необходимой при изготовлении бездымного пороха. В 1904 году был открыт метод управляемого синтеза окислов азота, который, однако, требовал огромного количества энергии. Так что природные селитры оставались основным источником связанного азота для химической промышленности, а также сельского хозяйства, где они используются в качестве удобрений. Благодаря открытию в 1913 году аммиачного метода связывания атмосферного азота, химическая промышленность смогла отказаться от дефицитного природного сырья. Сейчас вся азотная кислота производится методом растворения диоксида азота в воде в присутствии кислорода: 4NO2 + O2 + 2h3O → 4HNO3 Нитрат натрия, используемый в качестве азотного удобрения, получается при производстве азотной кислоты в процессе поглощения раствором соды остаточных окислов азота: Na2CO3 + NO2 → NaNO3 + NaNO2 + CO2↑ Таким образом, технология получения оксида азота (IV) позволила уменьшить расходы на сельское хозяйство и химическую промышленность. Говоря об азотной кислоте, нельзя также обойти вниманием интересное вещество под названием «царская водка». Оно представляет собой смесь из одного объёма концентрированной азотной кислоты HNO3 и трёх объёмов концентрированной соляной кислоты HCl. Царская водка обладает уникальными свойствами. В ней можно растворить благородные металлы, такие как золото, платина, палладий. Растворение происходит не только посредством окисления металлов кислотами, но и за счёт образования сложных растворимых соединений этих элементов. Не будем подробно рассматривать эти процессы, поскольку химия их сложна для восприятия. Помимо растворения благородных металлов, царская водка используется для получения довольно важного соединения – хлорида олова (IV): 4HCl + 2HNO3 + Sn → SnCl4 + NO2 + NO + 3h3O melscience.com NO2, "лисий хвост" или чем дышат жители Владикавказа по вине завода "Электроцинк".Продолжение.В продолжении темы о сернистом ангидриде (SO2) нужно обязательно рассказать ещё об одном опасном химическом соединении, которое периодически попадает в атмосферу нашего города по вине завода "Электроцинк". Я имею в виду диоксид азота (NO2). Следует обязательно указать на то, что это ещё более токсичное и опасное вещество, нежели чрезвычайно токсичный сернистый ангидрид. Для начала, выдержка из материалов дела, на которое указал один из моих собеседников drobilschik :"Управление Росприроднадзора по РСО-Алания использовало сведения станции «СКАТ», зафиксировавшей превышение в 1,7 раза ПДК по диоксиду серы в атмосферном воздухе по ул.Титова (территория больницы СОГМА) и протокол количественного химического анализа ФБУ «ЦЛАТИ» по РСО-Алания № 3 от 01.02.2012, из которого следует превышение в 1,6 раза ПДК по диоксиду серы в атмосферном воздухе по ул.Ставропольской 4, из которых следует, что 01.02.2012 в различных частях города в ходе контроля соблюдения нормативов ПДК были отобраны пробы воздуха. В результате количественного химического анализа установлено: по протоколам №1 превышение азота диоксида в 10,6 раз; по протоколу №3 превышение ПДК серы диоксида в 1,6 раз и азота диоксида в 2,1 раза; по протоколу №4 превышения ПДК по азота диоксида в 2,3 раза". Итак, что же это за вещество - диоксид азота и насколько оно опасно для жителей Владикавказа, когда попадает в атмосферу города ? Цитата из энциклопедии:---------------------------"Оксиды азота, улетучивающиеся в атмосферу, представляют серьёзную опасность для экологической ситуации, так как способны вызывать кислотные дожди, а также сами по себе являются токсичными веществами, вызывающими раздражение слизистых оболочек. Двуокись азота воздействует в основном на дыхательные пути и легкие, а также вызывает изменения состава крови, в частности, уменьшает содержание в крови гемоглобина. В специальной литературе также указывается на то, что воздействие на организм человека диоксида азота снижает сопротивляемость к заболеваниям, вызывает кислородное голодание тканей, особенно у детей. Усиливает действие канцерогенных веществ, способствуя возникновению злокачественных новообразований. Улетучивающиеся в атмосферу оксиды азота являются серьёзной опасностью для экологической ситуации, поскольку вызывают так называемые кислотные дожди. Но также они опасны сами по себе в силу своей токсичности, свойства вызывать раздражение слизистых оболочек человеческого организма."-------------------------------Снижает сопротивляемость организма к заболеваниям, изменяет состав крови, уменьшая содержание в крови гемоглобина, вызывает кислородное голодание тканей, усиливает действие канцерогенных веществ !!!! Когда идёт выброс именно NO2, то это хорошо видно в тёплое время суток по цвету газа из трубы Электроцинка. Газ оранжево-бурого цвета (так называемый "лисий хвост"). При низких температурах диоксид азота димеризуется и становится бесцветным. Т.е., как только из трубы завода-убийцы повалил бурый дым, можно быть уверенным - там точно есть в составе NO2, чрезвычайно токсичный диоксид азота. tim-karsanti.livejournal.com Диоксид азотаХимический элемент азот с порядковым номером 7 расположен в 5 группе периодической системы Менделеева. Этот двухатомный газ при нормальных условиях достаточно инертен. В земной атмосфере на его долю приходится три четверти. Элемент характеризуется следующими степенями окисления: −3, −1, 0, 1, 2, 3, 4, 5. Он входит в состав многих соединений. Одним из них является красновато-коричневый ядовитый газ (отличается способностью раздражать дыхательные пути, вызывает отек легких при больших концентрациях), имеющий характерный резкий, едкий запах — это диоксид азота. Формула имеет вид NO2. Молярная масса 46,01 г/моль. Плотность 2,62 г/дм³. Температура кипения 21 °C. При растворении в воде реагирует с ней. Показатель преломления 1,449 (при 20 ° C). Диоксид азота играет важную роль в химии атмосферы, в том числе в формировании тропосферного озона. Одновременно он является крупным загрязнителем воздуха и промежуточным продуктом в промышленном синтезе азотной кислоты, миллионы тонн которой производятся каждый год. Это один из нескольких оксидов азота (бинарные неорганические соединения азота с кислородом) со степенями окисления:
Диоксид азота легко сжижается. Он тяжелее воздуха. При нормальных условиях NO2 смешан (примерно, 1:1) с бесцветным веществом (своим димером) N2O4. Химия NO2 хорошо изучена. При взаимодействии с водой гидролизуется, в результате образуются две кислоты (азотистая и азотная): 2NO2 + h3O → HNO2 + HNO3. В реакциях со щелочами образуются соли этих же двух кислот: 2NaOH + 2NO2 → NaNO2 + NaNO3 + h3O. Он является сильным окислителем, способен окислять SO2 до SO3. На этом его свойстве основан метод нитрозного получения серной кислоты. В среде NO2 многие вещества, включая органические соединения, серу, уголь и фосфор, горят. Диоксид азота обычно образуется в результате окисления оксида азота кислородом воздуха: O2 + 2NO → 2NO2 В лаборатории NO2 получают в два этапа: дегидратацией азотной кислоты до пентаоксида диазота, который затем разлагают термическим путем: 2HNO3 → N2O5 + h3O, 2N2O5 → 4NO2 + O2. В результате термического разложения нитратов некоторых металлов также можно получить NO2: 2Pb(NO3)2 → 4NO2 + 2PbO + O2. Окисел может образовываться при взаимодействии азотной кислоты (концентрированной) с металлами (например, медью): 4HNO3 + Cu → 2NO2 + Cu(NO3)2 + 2h3O. При воздействии азотной кислоты (концентрированной) на олово, кроме диоксида азота, образуется оловянная кислота в качестве побочного продукта: 4HNO3 + Sn → h3O + h3SnO3 + 4NO2. В некоторых источниках окисел N2O4(IV) называют не иначе, как тетраоксид азота. Но это неправильное название, так как вещество является тетраоксидом диазота. NO2 существует в равновесии с бесцветным газом N2O4: 2NO2↔N2O4. Так как это равновесие является экзотермическим, то оно сдвигается в сторону NO2 при более высоких температурах, а при более низких — в сторону N2O4. Димер переходит в твердое состояние при температуре минус 11,2 оС. При температуре 150 градусов разлагается: N2O4 → 2NO2, затем 2NO2 → 2NO + O2. Азотная кислота медленно выделяет NO2, который придает характерный желтый цвет большинству образцов этой кислоты: 4HNO3 → 4NO2 + 2h3O + O2. Диоксид азота легко обнаружить по запаху уже при низких концентрациях, вдыхания его паров лучше избегать. Одним из потенциальных источников NO2 является дымящая азотная кислота, которая выделяет NO2 при температурах выше 0 градусов. Симптомы отравления (отек легких), как правило, появляются после вдыхания потенциально смертельных доз через несколько часов. Существует ряд доказательств, что долгосрочное воздействие NO2 при концентрациях выше 40—100 мкг/м³ может снизить функцию легких и увеличить риск респираторных симптомов. В исследованиях некоторых ученых установлена связь между концентрацией NO2 и синдромом внезапной детской смерти. Диоксид азота образуется в большинстве процессов горения, где используется воздух в качестве окислителя. При повышенных температурах азот соединяется с кислородом с образованием оксида азота: O2 + N2 → 2NO, затем NO окисляется на воздухе с образованием диоксида O2 + 2NO → 2NO2:
fb.ru Оксиды азотаОксиды азотаПри описании свойств азота отмечалось, что при непосредственном взаимодействии азота с кислородом образуется только оксид азота (II) NO. Однако существуют оксиды азота со всеми возможными степенями окисления (от +1 до +5).
N2O - оксид азота (I), «веселящий газ»При обычной температуре N2O - бесцветный газ со слабым приятным запахом и сладковатым вкусом; обладает наркотическим действием, вызывая сначала судорожный смех, затем - потерю сознания. Способы получения1. Разложение нитрата аммония при небольшом нагревании: Nh5NO3 = N2O↑ + 2Н2О 2. Действие HNO3 на активные металлы 10HNO3(конц.) + 4Са = N2O↑ + 4Ca(NO3)2 + 5Н2О Химические свойстваN2O не проявляет ни кислотных, ни основных свойств, т. е. не взаимодействует с основаниями, с кислотами, с водой (несолеобразующий оксид). При Т > 500'С разлагается на простые вещества. N2O - очень сильный окислитель. Например, способен в водном растворе окислить диоксид серы до серной кислоты: N2O + SO2 + Н2О = N2↑ + h3SO4 NO - оксид азота (II), монооксид азота.При обычной температуре NO - бесцветный газ без запаха, малорастворимый в воде, очень токсичный (в больших концентрациях изменяет структуру гемоглобина). Способы получения1. Прямой синтез из простых веществ может быть осуществлен только при очень высокой Т: N2 + O2 = 2NО - Q 2. Получение в промышленности (1-я стадия производства HNO3). 4Nh4 + 5O2 = 4NО + 6Н2О 3. Лабораторный способ - действие разб. HNO3 на тяжелые металлы: 8HNO3 + 3Cu = 2NO + 3Cu(NO3)2 + 4Н2О Химические свойстваNO - несолеобразующий оксид (подобно N2О). Обладает окислительно-восстановительной двойственностью. 2NO + SO2 + Н2О = N2O↑ + h3SO4 2NO + 2h3 = N2 + 2Н2О (со взрывом) 2NO + O2 = 2NO2 10NO + 6KMnO4 + 9h3SO4 = 10HNO3 + 3K2SO4 + 6MnSO4 + 4Н2О NO2 - оксид азота (IV), диоксид азотаПри обычной температуре NO2 - красно-бурый ядовитый газ с резким запахом. Представляет собой смесь NO2 и его димера N2O4 в соотношении -1:4. Диоксид азота хорошо растворяется в воде. Способы полученияI. Промышленный - окисление NO: 2NO + O2 = 2NO2 II. Лабораторные: действие конц. HNO3 на тяжелые металлы: 4HNO3 + Сu = 2NO2↑ + Cu(NO3)2 + 2Н2О разложение нитратов: 2Pb(NO3)2 = 4NO2↑ + O2↑ + 2РbО Химические свойстваNO2 взаимодействует с водой, основными оксидами и щелочами. Но реакции протекают не так, как с обычными оксидами - они всегда окислительно - восстановительные. Объясняется это тем, что не существует кислоты со С.О. (N) = +4, поэтому NO2 при растворении в воде диспропорционирует с образованием 2-х кислот - азотной и азотистой: 2NO2 + Н2О = HNO3 + HNO2 Если растворение происходит в присутствии O2, то образуется одна кислота - азотная: 4NO2 + 2Н2О + O2 = 4HNO3 Аналогичным образом происходит взаимодействие NO2 со щелочами: в отсутствие O2: 2NO2 + 2NaOH = NaNO3 + NaNO2 + Н2О в присутствии O2: 4NO2 + 4NaOH + O2 = 4NaNO3 + 2Н2О По окислительной способности NO2 превосходит азотную кислоту. В его атмосфере горят С, S, Р, металлы и некоторые органические вещества. При этом NO2 восстанавливается до свободного азота: 10NO2 + 8P = 5N2 + 4P2O5 2NO2 + 8HI = N2 + 4I2 + 4Н2О (возникает фиолетовое пламя) В присутствии Pt или Ni диоксид азота восстанавливается водородом до аммиака: 2NO2 + 7Н2 = 2Nh4 + 4Н2О Как окислитель NO2 используется в ракетных топливах. При его взаимодействии с гидразином и его производными выделяется большое количество энергии: 2NO2 + 2N2h5 = 3N2 + 4Н2О + Q N2O3 и N2O5 - неустойчивые веществаОба оксида имеют ярко выраженный кислотный характер, являются соответственно ангидридами азотистой и азотной кислот. N2O3 как индивидуальное вещество существует только в твердом состоянии ниже Т пл. (-100С). С повышением температуры разлагается: N2O3 → NO + NO2 N2O5 при комнатной температуре и особенно на свету разлагается так энергично, что иногда самопроизвольно взрывается: 2N2O5 = 4NO2 + O2 examchemistry.com |
|
||||||||||||||||||
|
|
||||||||||||||||||
|