Ядовитый «лисий хвост» над Казанью: всё идет по плану. Лисий хвост газОксид азота (I, II, III, IV, V): свойства, получение, применениеВведение Если внимательно взглянуть на азот в периодической системе химических элементов Д. И. Менделеева, то можно заметить, что он имеет переменную валентность. Это значит, что азот образует сразу несколько бинарных соединений с кислородом. Некоторые из них были открыты недавно, а некоторые - изучены вдоль и поперек. Существуют малостабильные и устойчивые оксиды азота. Химические свойства каждого из этих веществ совершенно разные, поэтому при их изучении нужно рассматривать как минимум пять оксидов азота. Вот о них и пойдет речь в сегодняшней статье. Оксид азота (I)
Свойства В обычных условиях представлен бесцветным газом, имеющим сладковатый запах. Его могут растворять вода, этанол, эфир и серная кислота. Если газобразный оксид одновалентного азота нагреть до комнатной температуры под давлением 40 атмосфер, то он сгущается до бесцветной жидкости. Это несолеобразующий оксид, разлагающийся во время нагревания и показывающий себя в реакциях как восстановитель. Получение Этот оксид образуется, когда нагревают сухой нитрат аммония. Другой способ его получения - термическое разложение смеси "сульфаминовая + азотная кислота". Применение Используется в качестве средства для ингаляционного наркоза, пищевая промышленность знает этот оксид как добавку E942. С его помощью также улучшают технические характеристики двигателей внутреннего сгорания. Оксид азота (II)
Свойства При нормальных условиях имеет вид бесцветного газа, который плохо растворяется в воде. Его трудно сжижить, однако в твердом и жидком состояниях это вещество имеет голубой цвет. Данный оксид может окисляться кислородом воздуха Получение Его довольно просто получить, для этого нужно нагреть до 1200-1300оС смесь азота и кислорода. В лабораторных условиях он образуется сразу при нескольким опытах:
Применение Это одно из веществ, из которых получают азотную кислоту. Оксид азота (III)
Свойства В нормальных условиях является жидкостью, которая имеет синий цвет, а в стандартных - бесцветным газом. Чистый оксид существует только в твердом агрегатном состоянии. Получение Образуется при взаимодействии 50%-ной азотной кислоты и твердого оксида трехвалентного мышьяка (его также можно заменить крахмалом). Применение С помощью этого вещества в лабораториях получают азотистую кислоту и ее соли. Оксид азота (IV)
Свойства Последнее название соответствует одному из его свойств. Ведь этот оксид имеет вид или красно-бурого газа или желтоватой жидкости. Ему присуща высокая химическая активность. Получение Данный оксид получают при взаимодействии азотной кислоты и меди, а также во время термического разложения нитрата свинца. Применение С помощью него производят серную и азотную кислоты, окисляют жидкое ракетное топливо и смесевые взрывчатые вещества. Оксид азота (V)
Свойства Имеет вид бецветных и очень летучих кристаллов. Они могут плавиться при температуре 32,3оС. Получение Этот оксид образуется при нескольких реакциях:
Применение Из-за своей крайней неустойчивости в чистом виде нигде не используется. Заключение В химии существует девять оксидов азота, приведенные выше являются только классическими соединениями этого элемента. Остальные четыре - это, как уже было сказано, нестабильные вещества. Однако их все объединяет одно свойство - высокая токсичность. Выбросы оксидов азота в атмосферу приводят к ухудшению состояния здоровья живущих поблизости от промышленных химических предприятий людей. Симптомы отравления каким-либо из этих веществ - токсический отек легких, нарушение работы центральной нервной системы и поражение крови, причина которого - связывание гемоглобина. Поэтому с оксидами азота необходимо осторожно обращаться и в большинстве случаев использовать средства защиты. fb.ru Ядовитый «лисий хвост» над Казанью: всё идет по плану Облако оранжево-бурого цвета появилось в четверг около полудня в небе над Казанским пороховым заводом. В соцсетях тут же появились сообщения жителей Кировского района, что в воздухе - резкий кислый запах, от которого першит в горле. Пресс-служба МЧС РТ отреагировала на происшествие удивительно быстро. В 12.07 на сайте ведомства было опубликовано официальное сообщение, что «желтый дым», который появился над Казанским пороховым заводом - это «выброс оксида азота, последствия разложения нитроцеллюлозы, применяемой при производстве пороха». Как уверяет МЧС, «опасности для жизни и здоровья горожан подобные выбросы не представляют, являются частью технологического процесса». Более того, выброс оксида азота, по данным МЧС, был плановый и был предварительно согласован с Роспотребнадзором и Росприроднадзором. В общем, без паники, казанцы!.. Однако, по мнению экологов-общественников, появившийся сегодня в казанском небе «лисий хвост» - это не просто оксид азота, а ядовитый диоксид. Действительно, на уроках химии в школе учат, что только один из оксидов азота имеет характерный цвет «лисьего хвоста» - это ядовитый NO2, имеющий второй класс опасности. То, что над пороховым заводом поднялось сегодня облако именно ядовитого диоксида азота, «Вечерней Казани» подтвердил известный эколог-общественник, доцент кафедры химической кибернетики КНИТУ-КХТИ Сергей Мухачев. - На пороховом заводе применяют реакцию нитрования. Во время этой реакции и выделяется диоксид азота, который, попадая в атмосферу, образует азотистую кислоту, - объяснил Мухачев. - Диоксид азота раздражает дыхательные пути человека, а в больших концентрациях может вызвать даже отек легких. Наиболее чувствительны к диоксиду азота маленькие дети. Выбросы этого газа способны вызвать резкий рост легочных заболеваний у них. - Когда люди видят в небе «лисий хвост», это значит, что концентрация газа намного превышает предельно допустимые нормы, - продолжает Сергей Мухачев. - Появление в небе облака диоксида азота может свидетельствовать о том, что на предприятии возникла аварийная ситуация. Однако, если верить сообщению МЧС РТ, зловещий «хвост» не имеет отношения к аварии: «Столь необычные последствия регламентных работ, по объяснению представителей Казанского порохового завода, связаны со сложившимися метеоусловиями. Летом в ясную солнечную погоду они более заметны». Зампредседателя татарстанского отделения Всероссийского общества охраны природы Татьяна Лядова сообщила «Вечерней Казани», что Казанский пороховой завод регулярно делает выбросы диоксида азота в атмосферу, но, как правило, в темное время суток, а также по выходным, когда надзорные органы отдыхают. www.evening-kazan.ru азот, хлор, бром, йод, оксид азота 2, лисий хвост(NO2), угарный газ? — 22 ответа No2 цветВ разделе Естественные науки на вопрос как распознать газы: азот, хлор, бром, йод, оксид азота 2, лисий хвост(NO2), угарный газ? заданный автором Анна лучший ответ это Легко. Среди перечисленных Вами веществ, бром - единственная (довольно летучая) жидкость красно-коричневого цвета; иод - кристаллы темного цвета. Если взять немного иода в пробирку и нагреть её - можно увидеть красивые пары фиолетового цвета. Все остальные вещества - газы (в нормальных условиях). Из них единственный газ - горючий, это CO (угарный газ) ; он легко воспламеняется: 2 CO + O2 = 2 CO2. Остальные газы (азот, Cl2, NO и NO2) не "горят". Более точно выражаясь, NO в принципе окисляется кислородом, но для этого нужны весьма жёсткие условия: высокая температура и катализатор. Из этих четырёх газов легко распознается хлор. Если его много - он дает зеленовато-желтую окраску, если мало - выглядит бесцветным. Но в любом случае распознать его очень просто. Возьмите бумажку, смоченную раствором иодида калия и пропустите через неё хлор - бумага быстро потемнеет из-за выделившегося иода (KI + Cl2 = KCl + I2). Нет особых проблем и с NO2 - во-первых, он оранжево-желтого цвета (из-за образующихся димеров N2O4). Во-вторых, некоторое количество этого газа следует растворить в воде. Тогда пройдёт реакция диспропорционирования, NO2 + h3O = HNO2 + HNO3, и кислый характер раствора Вы без труда определите с помощью индикатора. Осталось два газа - N2 и NO. Если NO пропустить через водный раствор FeSO4, то раствор почернеет: образуются комплексы [Fe(NO)(h3O)5](2+). Ну и, наконец, остался единственный газ - N2. Для того, чтобы окончательно убедиться, что это азот, направьте поток этого газа на горящую спичку - она погаснет... Ответ от 2 ответа[гуру]Привет! Вот подборка тем с ответами на Ваш вопрос: как распознать газы: азот, хлор, бром, йод, оксид азота 2, лисий хвост(NO2), угарный газ? Ответ от Иванька[гуру]Мне смешно, что Субач относит йод к металлам? странно? ведь это галоген, типичнейший неметалл.Еще главное с иронией говорит, странно где он получал образование, иод-металл (умру со смеху)Так вот Аня: начни с хлора: резкий удушливый запах,лисий хвост - рыжый цвет, эти газы можно распознать по физическим свойствам, остальные же нужно химически:ну бром, это жидкость, бурого цвета, зловонна, йод - кристаллы черного цвета, если в р-ре то бурый раствор, светлее чем бром, угарный газ, достаточно пропустить над черным порошком оксида меди (II) получаем медь, красного цвета, оксид азота (II) NO и азот (N2) это два бесцветных газа, азот методом исключения, но монооксид азота по реакции Ответ от Ёубач Андрей[гуру]Солнце, с каких пор йод стал газом? Открой таблицу Д. И. Менделеева, и будет тебе откровение, что йод это металл! Ответ от 2 ответа[гуру]Привет! Вот еще темы с нужными ответами:
Ответить на вопрос:22oa.ru азот, хлор, бром, йод, оксид азота 2, лисий хвост(NO2), угарный газ?Легко. Среди перечисленных Вами веществ, бром - единственная (довольно летучая) жидкость красно-коричневого цвета; иод - кристаллы темного цвета. Если взять немного иода в пробирку и нагреть её - можно увидеть красивые пары фиолетового цвета. Все остальные вещества - газы (в нормальных условиях) . Из них единственный газ - горючий, это CO (угарный газ) ; он легко воспламеняется: 2 CO + O2 = 2 CO2. Остальные газы (азот, Cl2, NO и NO2) не "горят". Более точно выражаясь, NO в принципе окисляется кислородом, но для этого нужны весьма жёсткие условия: высокая температура и катализатор. Из этих четырёх газов легко распознается хлор. Если его много - он дает зеленовато-желтую окраску, если мало - выглядит бесцветным. Но в любом случае распознать его очень просто. Возьмите бумажку, смоченную раствором иодида калия и пропустите через неё хлор - бумага быстро потемнеет из-за выделившегося иода (KI + Cl2 = KCl + I2). Нет особых проблем и с NO2 - во-первых, он оранжево-желтого цвета (из-за образующихся димеров N2O4). Во-вторых, некоторое количество этого газа следует растворить в воде. Тогда пройдёт реакция диспропорционирования, NO2 + h3O = HNO2 + HNO3, и кислый характер раствора Вы без труда определите с помощью индикатора. Осталось два газа - N2 и NO. Если NO пропустить через водный раствор FeSO4, то раствор почернеет: образуются комплексы [Fe(NO)(h3O)5](2+). Ну и, наконец, остался единственный газ - N2. Для того, чтобы окончательно убедиться, что это азот, направьте поток этого газа на горящую спичку - она погаснет... Солнце, с каких пор йод стал газом? Открой таблицу Д. И. Менделеева, и будет тебе откровение, что йод это металл! Мне смешно, что Субач относит йод к металлам? странно? ведь это галоген, типичнейший неметалл. Еще главное с иронией говорит, странно где он получал образование, иод-металл (умру со смеху) Так вот Аня: начни с хлора: резкий удушливый запах, лисий хвост - рыжый цвет, эти газы можно распознать по физическим свойствам, остальные же нужно химически: ну бром, это жидкость, бурого цвета, зловонна, йод - кристаллы черного цвета, если в р-ре то бурый раствор, светлее чем бром, угарный газ, достаточно пропустить над черным порошком оксида меди (II) получаем медь, красного цвета, оксид азота (II) NO и азот (N2) это два бесцветных газа, азот методом исключения, но монооксид азота по реакции touch.otvet.mail.ru Лисий хвост газ - g.auteh.ruНа этой странице собраны фото по запросу Лисий хвост газ.Лисий хвост газ  Лисий хвост газ Лисий хвост газ Лисий хвост газ Лисий хвост газ  Лисий хвост газ  Лисий хвост газ Тэги:g.auteh.ru |
|
||||||||||||||||||
|
|
||||||||||||||||||
|




 Формула - N2O. Иногда его могут называть оксонитридом азота, оксидом диазота, закисью азота или веселящим газом.
Формула - N2O. Иногда его могут называть оксонитридом азота, оксидом диазота, закисью азота или веселящим газом. Формула - NO. Встречается под названиями монооксида азота, окиси азота и нитрозил-радикала
Формула - NO. Встречается под названиями монооксида азота, окиси азота и нитрозил-радикала Формула - N2O3. Также его могут называть азотистым ангидридом и сесквиоксидом азота.
Формула - N2O3. Также его могут называть азотистым ангидридом и сесквиоксидом азота.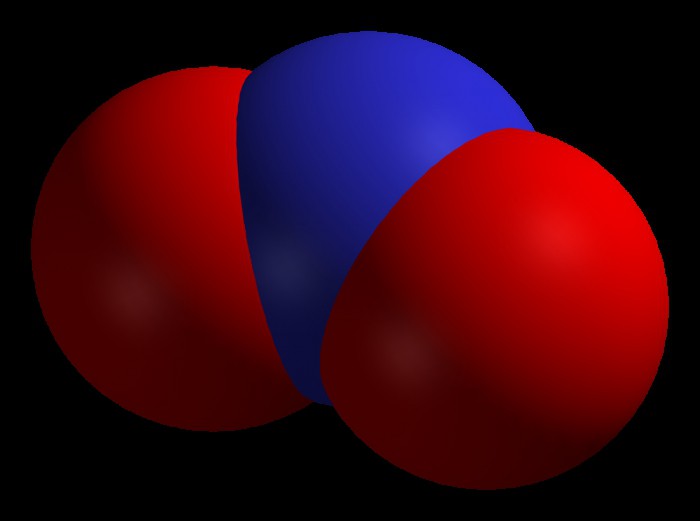 Формула - NO2. Также его могут называть диоксидом азота или бурым газом.
Формула - NO2. Также его могут называть диоксидом азота или бурым газом. Формула - N2O5. Может встречаться под названиями пентаоксида диазота, нитрата нитроила или азотного ангидрида.
Формула - N2O5. Может встречаться под названиями пентаоксида диазота, нитрата нитроила или азотного ангидрида.