Большая Энциклопедия Нефти и Газа. Процесс горения топливаПроцесс горения топлива | Теория горения топливаЗдравствуйте! Основной качественной характеристикой процесса горения является химическая его полнота при минимальном избытке воздуха, которому соответствует наибольшая температура горения. Горение представляет собой быстро протекающее химическое превращение, сопровождающееся выделением теплоты. К процессам горения относят не только окислительные реакции горения, но и все химические процессы, связанные с быстрым превращением исходных продуктов и тепловым и диффузионным ускорением (разложение взрывчатых веществ, озона, соединение ряда веществ с хлором и фтором и др.). Химическая реакция горения в большинстве случаев является сложной, то есть состоит из нескольких элементарных химических процессов, в которых образуются промежуточные продукты реакции. Кроме того, при горении происходят различные физические процессы (перенос теплоты, диффузия, движение и смесеобразование реагирующих веществ, испарение топлива и т. д.), интенсивность протекания которых влияет на скорость горения. Реакция горения обладает свойством самоускорения вследствие накопления в системе теплоты, а также активных продуктов реакции. При этом увеличение скорости реакции w = —dC/dτ, характеризующей изменение концентрации реагирующего вещества С во времени τ , будет происходить до тех пор, пока в системе не установятся определенные значения параметров (температура, давление, состав смеси). В зависимости от факторов, замедляющих скорость реакции, различают кинетическое и диффузионное горение. Если скорость горения газовой смеси лимитируется факторами, влияющими на кинетику химической реакции {концентрацией, температурой, давлением), то такое горение называют кинетическим. При раздельной подаче топлива и окислителя скорость горения ограничивается факторами, которые определяют интенсивность перемешивания (скорость и турбулизация потоков, конфигурация и взаимное расположение каналов, по которым подводятся топлива и окислитель и др.). В этом случае горение называют диффузионным. При этом для увеличения скорости смесеобразования применяют меры по турбулизации потока. Скорость реакции горения смеси газов, согласно закону действующих масс, пропорциональна произведению концентраций СА и СВ реагирующих веществ А и В:
Коэффициент пропорциональности k называется константой скорости реакции. Согласно уравнению, приведенному выше, вероятность столкновения молекул реагирующих веществ пропорциональна произведению их концентраций. Константа скорости реакции зависит от температуры Т и определяется из уравнения Аррениуса
где k0 — коэффициент, определяемый экспериментально; Rμ — универсальная газовая постоянная. Величина Е характеризует наименьшую избыточную энергию (по сравнению со средним значением кинетической энергии), которой должны обладать сталкивающиеся частицы, для того, чтобы разрушились внутримолекулярные связи и произошло химическое превращение. Эта величина, зависящая от природы реагирующих веществ, называется энергией активации (измеряется в кДж/кммоль). Из выражений (1) и (2) следует, что с увеличением энергии активации константа скорости и скорость реакции уменьшаются. С увеличением температуры скорость реакции возрастает, что объясняется увеличением кинетической энергии реагирующих молекул и вероятности их столкновений с ростом температуры. Вероятность столкновения и скорость реакции возрастают также с увеличением давления в системе. Экспериментальные исследования показывают, что энергия активации значительно меньше, чем по классическим законам химической кинетики (закон действующих масс, уравнение Аррениуса). Это отклонение объясняется на основе теории цепных реакций. Согласно этой теории, процесс горения протекает через промежуточные стадии с непрерывным образованием активных центров реакции. Например, при горении водорода активными центрами являются свободные атомы Н и О и радикалы ОН, которые относительно легко вступают в дальнейшие взаимодействия. При этом энергия активации для реакций с участием активных центров меньше, чем для молекул реагирующих веществ. Цепные реакции являются разветвленными процессами, в которых каждое взаимодействие одного активного центра приводит к образованию нескольких активных центров. Процессу горения всегда предшествует воспламенение топлива. Окислительные процессы в смеси газов могут происходить и при низких температурах, но в этом случае количество выделяемой теплоты невелико. Теплота успевает перейти из системы в окружающую среду, и реакция не ускоряется. При увеличении температуры смеси, согласно уравнению Аррениуса (2), увеличивается скорость реакции, и при некоторой температуре количество выделяемой теплоты превысит тепловые потери в окружающую среду, что приведет к воспламению топлива. Минимальная температура, при которой смесь воспламеняется, называется температурой воспламенения. Температура воспламенения не является физико-химической константой вещества. Она зависит как от рода газа, так И от концентрации газа и окислителя, а также от интенсивности теплообмена между газом и окружающей средой. Из горючих газов наибольшую температуру воспламенения имеет метан Ch5 (650—750° С) и наименьшую — ацетилен С2Н2 (400—440° С). Существуют верхний и нижний пределы концентрации газа и окислителя, и вне этих пределов смеси не воспламеняются. Например, для смеси метана и воздуха при температуре 20° С и давлении 0,1 МПа нижний предел равен 5 — 6% и верхний-12 — 15%, для смеси водорода с воздухом эти пределы соответственно равны 4 — 9% и 65-75%. С увеличением температуры смеси пределы воспламенения значительно расширяются. Смеси, концентрация которых находится в пределах воспламенения, взрывоопасны , такт как при постоянном объеме они сгорают практически мгновенно (детонируют). Если при горении смесь может беспрепятственно расширяться (горение при потсоянном давлении), то пламя обычно распространяется с небольшой скоростью (менее 30 м/с). Такое горение принято называть нормальным горением. Скорость распространения пламени в этом случае зависит от природы и температуры смеси, а также от концентрации реагирующих и инертных компонентов смеси. При нормальном горении в зависимости от характера движения горючего газа и окислителя пламя может быть ламинарным и турбулентным. Ламинарное пламя встречается в малопроизводительных атмосферных горелках. В технике чаще всего сжигание газообразного топлива производят в турбулентном потоке. При турбулентном горении длина и конфигурация пламени существенно зависят от конструкции горелочного устройства. Исп. литература: 1) Хзмалян Д.М., Каган Я.А. Теория горения и топочные устройства, Москва, «Энергия», 1976; 2)Теплотехника, Бондарев В.А., Процкий А.Е., Гринкевич Р.Н. Минск, изд. 2-е,"Вышейшая школа", 1976. teplosniks.ru Горение топлива.Топливо и его горениеТопливом называют горючие вещества, применяемые для получения теплоты (тепловой энергии) при их сжигании. Под сжиганием обычно подразумевают окисление горючих веществ кислородом воздуха. Промышленным топливом считаются не все горючие вещества, а лишь те, которые удовлетворяют следующим требованиям:
Топливо, добываемое из недр земли в готовом виде, называют естественным, а получаемое путем переработки горючих веществ и природного топлива – искусственным. Как естественное, так и искусственное топливо подразделяют на твердое, жидкое и газообразное. В качестве примера естественных твердых топлив можно привести ископаемый уголь, торф, горючие сланцы, дрова, отходы сельскохозяйственного производства. Искусственное твердое топливо – кокс, полукокс, пылевидное топливо, брикеты, древесный уголь. К естественному жидкому топливу относится нефть, а к искусственному – получаемые из нефти продукты – бензин, керосин, дизельное топливо, газойль, мазут, нефтяное и котельное топливо. По назначению топливо подразделяют на энергетическое и технологическое. К энергетическим относят все низкосортные топлива, которые можно сжигать на электростанциях, в производственно-бытовых и других тепловых установках в натуральном виде или после переработки. Это антрацит, бурые угли, торф, природный газ, а также продукты переработки других топлив. К технологическому топливу относят высокосортное топливо и коксующиеся угли. По методу добычи и потребления различают местное и привозное топливо. *** Составные части топливаТопливо состоит из органической и минеральной частей. Органическую часть топлива составляют следующие химические элементы: углерод (С), водород (Н2), кислород (О2), азот (N2) и сера (S). Топливо может состоять из смеси этих элементов или только их части. Так, органическую массу кокса или древесного угля в основном составляет углерод, а нефтепродуктов и газового топлива – углерод, водород и кислород. Наиболее ценные из перечисленных элементов топлива – углерод и водород. Кислород и азот являются внутренним балластом топлива, поскольку они не горят. Сера является нежелательным компонентом топлива, несмотря на то, что сгорая, она выделяет теплоту. При сгорании этого элемента образуется сернистый газ и серная кислота, пагубно влияющие на экологию и вызывающие сильную коррозию металлов. Минеральная часть топлива составляют вода и минеральные примеси, которые являются внешней балластной частью (внешним балластом) топлива. Содержание балластной части в топливе очень нежелательно, поскольку увеличивая массу и объем топлива, она уменьшает его тепловую ценность. Минеральные составляющие после сжигания образуют твердый остаток – золу. *** Сущность процесса горенияГорение есть окисление горючих элементов топлива кислородом, сопровождающееся выделением теплоты. В зависимости от скорости распространения пламени различают нормальное горение и горение со взрывом. При нормальном горении скорость распространения пламени равна 15-25 м/с, а при взрывном горении – 2000-3000 м/с. Чтобы топливо начало гореть, его необходимо нагреть до определенной температуры, называемой температурой воспламенения. Так, например, каменный уголь воспламеняется при температуре 225-375 ˚С, сухой торф – 225-300 ˚С, дрова – 350-450 ˚С, керосин – 380 ˚С, бензин – 415 ˚С, метан (СН4) – 650-700 ˚С и т. д. При нагревании топлива до температуры воспламенения начинается распад горючей массы на составные элементы, которые затем окисляются кислородом и выделяют теплоту. Эта теплота способствует нагреву массы близлежащего топлива, в которых начинают протекать аналогичные процессы (распад и окисление), и, таким образом, вся масса топлива, находящегося в топке, начинает гореть. Для того, чтобы процесс горения не прекратился, выделяющаяся теплота должна поддерживать температуру топлива не ниже температуры воспламенения. Горение может быть полным и неполным. Полным горением называют процесс окисления горючих элементов топлива кислородом, при котором выделяются продукты, не способные гореть в дальнейшем. Неполное сгорание топлива сопровождается выделением продуктов горения, которые в дальнейшем могут воспламеняться и сгорать повторно. Так, при полном сгорании углерода выделяется углекислый газ СО2, который в дальнейшем гореть не способен. Однако, если углерод сгорает при недостаточном количестве кислорода, то продуктом его окисления является углекислота СО, которая может загореться при соответствующих условиях. При этом неполное горение сопровождается выделением значительно меньшего количества теплоты, т. е. считается нежелательным явлением. Для того чтобы процесс горения был полным, необходимо обеспечить подачу достаточного количества воздуха (содержащего кислород) в зону горения. На практике, сжигая топливо, стараются придерживаться определенного баланса между количеством воздуха и топлива, поскольку избыток воздуха сопровождается потерями теплоты на его подогрев. *** Количество воздуха, необходимое для полного сгорания топливаКоличество воздуха, необходимое для полного сгорания топлива, определить несложно, если известно процентное содержание в топливе основных горючих элементов – углерода, водорода, серы и кислорода. Так как атомная масса углерода 12, а кислорода – 16, то для получения углекислого газа СО2 необходимо 12 частей углерода соединить с 32 частями кислорода, т. е. на одну массовую долю углерода должно приходиться 2,67 частей кислорода. Зная атомную массу водорода и серы, а также формулы продуктов их полного окисления, можно аналогично рассчитать необходимое количество кислорода для сжигания 1 части любого горючего элемента. При определении количества воздуха, необходимого для полного горения, следует учитывать, что в топливе тоже содержится некоторое количество кислорода, а также то, что массовая доля кислорода в воздухе - 23,2 %. В общем случае формула для определения массового количества воздуха для полного сгорания топлива имеет вид: mT = (2,67Ср + 8Нр + Sр – Ор)/0,232, где: Ср, Нр, Sр, Ор – соответственно массовое содержание углерода, водорода, серы и кислорода в топливе. При сгорании топлива часть кислорода воздуха не успевает вступить в реакцию окисления, поэтому для обеспечения полного сгорания топлива следует к нему подводить воздух с некоторым избытком по сравнению с теоретически необходимым количеством. Отношение действительного количества воздуха к теоретически необходимому количеству называют коэффициентом избытка воздуха. На практике этот коэффициент (в зависимости от вида топлива) может принимать значения от 1,05 (газообразное и пылевидное топливо) до 1,8 (твердое топливо). *** Теплота сгорания топливаВажнейшая характеристика топлива – теплота его сгорания – количество теплоты, выделившейся при полном сгорании единицы количества топлива (для жидких и твердых топлив – кг, для газообразных – м3). Различают высшую и низшую теплоту сгорания. Высшей теплотой сгорания Qв называют теплоту, выделяемую при полном сгорании единицы количества топлива, в результате которого образующаяся влага конденсируется и выделяется в виде жидкости из продуктов сгорания. Если в результате сгорания единицы количества топлива образуемая влага остается в продуктах сгорания в парообразном состоянии, то выделяемую при этом теплоту называют низшей теплотой сгорания Qн. Эта величина меньше высшей теплоты сгорания топлива на теплоту парообразования (конденсации) влаги, образуемой при сжигании единицы количества топлива. Теплоту сгорания топлива, кДж/кг, можно определить опытным путем (при сжигании порции топлива в специальном приборе – калориметре) или расчетом (по формулам Менделеева), если известен элементарный состав топлива.Например, для твердого топлива: Qв = 339С + 1250Н – 108,85(О – S); для жидкого топлива: Qн = Qв – 25,1(9Нр + Wр), где: С, Н, О, S и W – соответственно процентное содержание углерода, водорода, кислорода, серы и влаги в рабочем топливе. *** Условное топливоПри расчете расхода топлива, а также топливных ресурсов пользуются понятием условное топливо. Это реальное топливо, теплота сгорания которого равна 29,3 МДж/кг. Для перевода любого топлива в условное, пользуются тепловым эквивалентом, который получается от деления теплоты Qрц сгорания данного топлива на теплоту сгорания условного топлива, т. е. на 29300 кДж/кг или 29,3 МДж/кг. Так, например, для торфа Эт = 8500/29300 = 0,29, т. е. 1 тонна торфа по своей тепловой ценности равноценна 0,29 тонны условного топлива. *** Температура горения топливаСледует различать теоретическую и действительную температуру горения.Теоретической температурой горения называют максимальную температуру, которую способно давать данное топливо при полном сгорании с теоретически необходимым количеством воздуха. Ее определяют опытным путем, или аналитически, используя формулы, в которых учитывается массовая доля и теплотворная способность каждого горючего элемента в топливе. При этом теоретическая температура горения будет равна отношению теплоты, полученной от сгорания единицы топлива, к сумме произведений массовых составляющих горючих элементов на их теплотворную способность. Теоретически определенная температура горения топлива всегда выше действительной, поскольку при расчетах не учитывается ее понижение из-за потерь теплоты на лучеиспускание, избыток воздуха при сжигании, неполное сгорание топлива и т. п. Действительная температура горения (при коэффициенте избытка воздуха равном 1,0): антрацита - 2270 ˚С, торфа – 1700 ˚С, мазута – 1125 ˚С, природного газа – 2000 ˚С. *** Способы сжигания топливаВ котельной практике известны слоевой, факельный и вихревой способы сжигания топлива. Слоевой способ сжигания топлива (рис. 1а) заключается в следующем. Загруженное в топку топливо распределяется ровным слоем по колосниковой решетке, через которую проходит воздух, встречающий на своем пути неподвижный или движущийся слой горящего топлива. При взаимодействии с топливом воздух превращается в газовоздушный поток, который, пройдя через топочное пространство, выходит наружу. Для предотвращения уноса топлива необходимо, чтобы вес частичек топлива был больше силы газовоздушного потока. Однако, при слишком больших размерах кусков топлива замедляется процесс горения и уменьшается количество теплоты, получаемой в единицу времени, поэтому оптимальный размер кусков – 20-30 мм. Основным достоинством слоевого способа сжигания твердого топлива является наличие на колосниках запаса горящего топлива, обеспечивающего устойчивость протекания процесса. Существенным недостатком этого способа является необходимость использования твердого топлива с оптимальными размерами кусков, что требует предварительной их сортировки и дробления.Факельный способ сжигания топлива (рис. 1б), в отличие от слоевого, заключается в том, что частицы топлива движутся вместе с газовоздушным потоком в топочном пространстве. Поэтому масса частиц должна быть как можно меньше, и они должны удерживаться в газовоздушном потоке. Этим обеспечивается очень тщательное перемешивание частичек топлива с воздухом, интенсивное их горение, получается более однородный, устойчивый факел горения и происходит наиболее полное выгорание горючих элементов, составляющих горючую массу топлива. Поэтому при факельном способе применяют твердое топливо в виде очень мелких частичек (пыли), размеры которых составляют доли миллиметра. Существенный недостаток этого способа – малая скорость обтекания частиц топлива газовоздушным потоком, которая не позволяет значительно увеличить интенсивность горения, а также большая чувствительность к изменению режима работы, поскольку в топочном пространстве постоянно находится небольшое количество (запас) топлива. Поэтому регулирование процесса возможно при одновременном изменении подачи топлива и воздуха. Вихревой способ сжигания топлива (рис. 1в) заключается в создании в топочном пространстве вихря, благодаря которому топливо, поступающее в топку, подхватывается газовоздушным потоком и движется вместе с ним по определенной траектории до полного выгорания горючих элементов из горючей массы. Вихревое движение топлива в газовоздушном потоке способствует более длительному нахождению топлива в топочном пространстве, что создает условия для полного сгорания частиц размером 3-5 мм и для получения более устойчивого горения, чем при факельном способе сжигания. *** Котлы и котельные установки Скачать теоретические вопросы к экзаменационным билетам по учебной дисциплине "Основы гидравлики и теплотехники" (в формате Word, размер файла 68 кБ) Скачать рабочую программу по учебной дисциплине "Основы гидравлики и теплотехники" (в формате Word): Скачать календарно-тематический план по учебной дисциплине "Основы гидравлики и теплотехники" (в формате Word): k-a-t.ru Основные стадии процесса горения топлива / НовостиГорение топлива - это процесс окисления горючих компонентов, происходящий при высоких температурах и сопровождающийся выделением тепла. Характер горения определяется множеством факторов, в том числе способом сжигания, конструкцией топки, концентрацией кислорода и т. д. Но условия протекания, продолжительность и конечные результаты топочных процессов в значительной мере зависят от состава, физических и химических характеристик топлива.
Состав топлива
К твердому топливу относят каменный и бурый уголь, торф, горючие сланцы, древесину. Эти виды топлив представляют собой сложные органические соединения, образованные в основном пятью элементами - углеродом С, водородом Н, кислородом О, серой S и азотом N. В состав топлива также входит влага и негорючие минеральные вещества, которые после сгорания образуют золу. Влага и зола - это внешний балласт топлива, а кислород и азот - внутренний.
Основным элементом горючей части является углерод, он обуславливает выделение наибольшего количества тепла. Однако, чем больше доля углерода в составе твердого топлива, тем труднее оно воспламеняется. Водород при сгорании выделяет в 4,4 раза больше тепла, чем углерод, но его доля в составе твердых топлив невелика. Кислород, не будучи теплообразующим элементом и связывая водород и углерод, снижает теплоту сгорания, поэтому является элементом нежелательным. Особенно велико его содержание в торфе и древесине. Количество азота в твердом топливе небольшое, но он способен образовывать вредные для окружающей среды и человека оксиды. Также вредной примесью является сера, она выделяет мало теплоты, но образующиеся оксиды приводят к коррозии металла котлов и загрязнению атмосферы.
Технические характеристики топлива и их влияние на процесс горения Важнейшими техническими характеристиками топлива являются: теплота сгорания, выход летучих веществ, свойства нелетучего остатка (кокса), зольность и влагосодержание.
Теплота сгорания топлива
Теплота сгорания - это количество тепла, выделяющееся при полном сгорании единицы массы (кДж/кг) или объема топлива (кДж/м3). Различают высшую и низшую теплоту сгорания. В высшую входит тепло, выделяемое при конденсации паров, которые содержатся в продуктах сгорания. При сжигании топлива в топках котлов уходящие дымовые газы имеют температуру, при которой влага находится в парообразном состоянии. Поэтому в этом случае применяют низшую теплоту сгорания, которая не учитывает теплоту конденсации водяных паров.
Состав и низшая теплота сгорания всех известных месторождений угля определены и приводятся в расчетных характеристиках.
Выход летучих веществ
При нагревании твердого топлива без доступа воздуха под воздействием высокой температуры сначала выделяются водяные пары, а затем происходит термическое разложение молекул с выделением газообразных веществ, получивших название летучих веществ.
Выход летучих веществ может происходить в интервале температур от 160 до 1100 °С, но в среднем – в области температур 400-800 °С. Температура начала выхода летучих, количество и состав газообразных продуктов зависят от химического состава топлива. Чем топливо химически старше, тем меньше выход летучих и выше температура начала их выделения.
Летучие вещества обеспечивают более раннее воспламенение твердой частицы и оказывают значительное влияние на горение топлива. Молодые по возрасту топлива - торф, бурый уголь - легко загораются, сгорают быстро и практически полностью. Наоборот, топливо с низким выходом летучих, например, антрацит, загорается труднее, горит намного медленнее и сгорает не полностью (с повышенной потерей тепла).
Свойства нелетучего остатка (кокса)
Твердая часть топлива, оставшаяся после выхода летучих, состоящая в основном из углерода и минеральной части, называется коксом. Коксовый остаток может быть в зависимости от свойств органических соединений, входящих в горючую массу: спекшимся, слабоспекшимся (разрушающимся при воздействии), порошкообразным. Антрацит, торф, бурые угли дают порошкообразный нелетучий остаток. Большинство каменных углей спекается, но не всегда сильно. Слипшийся или порошкообразный нелетучий остаток дают каменные угли с очень большим выходом летучих (42-45%) и с очень малым выходом (менее 17%).
Структура коксового остатка важна при сжигании угля в топках на колосниковых решетках. При факельном сжигании в энергетических котлах характеристика кокса не имеет большого значения.
Зольность
Твердое топливо содержит наибольшее количество негорючих минеральных примесей. Это прежде всего глина, силикаты, железный колчедан, но также могут входить закись железа, сульфаты, карбонаты и силикаты железа, оксиды различных металлов, хлориды, щелочи и т.д. Большая часть их попадает при добыче в виде пород, между которыми залегают пласты угля, но присутствуют и минеральные вещества, перешедшие в топливо из углеобразователей или в процессе преобразования его исходной массы.
При сжигании топлива минеральные примеси претерпевают ряд реакций, в результате которых образуется твердый негорючий остаток, называемый золой. Вес и состав золы не идентичны весу и составу минеральных примесей топлива.
Свойства золы играют большую роль в организации работы котла и топки. Ее частички, уносимые продуктами сгорания, при высоких скоростях истирают поверхности нагрева, а при малых скоростях отлагаются на них, что ведет к ухудшению теплопередачи. Зола, уносимая в дымовую трубу, способна нанести вред окружающей среде, во избежание этого требуется установка золоуловителей.
Важным свойством золы является ее плавкость, различают тугоплавкую (выше 1425 °С), среднеплавкую (1200-1425 °С) и легкоплавкую (менее 1200 °С) золу. Зола, прошедшая стадию плавления и превратившаяся в спекшуюся или сплавленную массу, называется шлаком. Температурная характеристика плавкости золы имеет большое значение для обеспечения надежной работы топки и поверхностей котла, правильный выбор температуры газов около этих поверхностей позволит исключить шлакование.
Влагосодержание
Влага - нежелательная составляющая топлива, она наряду с минеральными примесями является балластом и уменьшает содержание горючей части. Помимо этого, она снижает тепловую ценность, так как дополнительно требуются затраты энергии на ее испарение.
Влага в топливе может быть внутренней и внешней. Внешняя влага содержится в капиллярах или удерживается на поверхности. С химическим возрастом количество капиллярной влаги сокращается. Поверхностной влаги тем больше, чем меньше куски топлива. Внутренняя влага входит в органическое вещество.
Содержание влаги в топливе снижает теплоту его сгорания, ведет к увеличению его расхода. При этом увеличиваются объемы продуктов сгорания, потери теплоты с уходящими газами и снижается КПД котлоагрегата. Повышенная влажность в зимнее время приводит к смерзанию угля, затруднениям при размоле и уменьшению сыпучести.
Способы сжигания топлива в зависимости от вида топки
Основные виды топочных устройств:
Слоевые топки предназначены для сжигания крупнокускового твердого топлива. Они могут быть с плотным и кипящим слоем. При сжигании в плотном слое воздух для горения проходит через слой, не влияя на его устойчивость, то есть сила тяжести горящих частиц превышает динамический напор воздуха. При сжигании в кипящем слое благодаря повышенной скорости воздуха частицы переходят в состояние "кипения". При этом происходит активное перемешивание окислителя и топлива, благодаря чему интенсифицируется горение топлива.
В камерных топках сжигают твердое пылевидное топливо, а также жидкое и газообразное. Камерные топки подразделяются на циклонные и факельные. При факельном сжигании частицы угля должны быть не более 100 мкм, они сгорают в объеме топочной камеры. Циклонное сжигание допускает больший размер частиц, под влиянием центробежных сил они отбрасываются на стенки топки и полностью выгорают в закрученном потоке в зоне высоких температур.
Горение топлива. Основные стадии процесса
В процессе горения твердого топлива можно выделить определенные стадии: подогрев и испарение влаги, возгонка летучих и образование коксового остатка, горение летучих и кокса, образование шлака. Такое деление процесса горения относительно условно, так как хотя эти этапы протекают последовательно, частично они налагаются друг на друга. Так, возгонка летучих веществ начинается до окончательного испарения всей влаги, образование летучих идет одновременно с процессом их горения, так же как и начало окисления коксового остатка предшествует окончанию горения летучих, а дожигание кокса может идти и после образования шлака.
Время течения каждой стадии процесса горения в значительной мере определяется свойствами топлива. Дольше всего длится стадия горения кокса, даже у топлив с большим выходом летучих. Существенное влияние на продолжительность стадий процесса горения оказывают разнообразные режимные факторы и конструктивные особенности топки.
1. Подготовка топлива до воспламенения
Топливо, поступающее в топку, подвергается нагреванию, в результате чего при наличии влаги происходит ее испарение и подсушка топлива. Время, необходимое на подогрев и подсушку, зависит от количества влаги и температуры, с которой топливо подается в топочное устройство. Для топлив с большим содержанием влаги (торф, влажные бурые угли) стадия прогрева и подсушивания сравнительна продолжительна.
В слоевые топки топливо подают с температурой, приближенной к окружающей среде. Только в зимнее время в случае смерзания угля его температура ниже, чем в котельном помещении. Для сжигания в факельных и вихревых топках топливо подвергают дроблению и размолу, сопровождаемому сушкой горячим воздухом или дымовыми газами. Чем выше температура поступающего топлива, тем меньше времени и тепла необходимо на подогрев его до температуры воспламенения.
Подсушка топлива в топке происходит за счет двух источников тепла: конвективного тепла продуктов сгорания и лучистого тепла факела, обмуровки, шлака.
В камерных топках подогрев осуществляется преимущественно за счет первого источника, то есть подмешивания к топливу продуктов сгорания в месте его ввода. Поэтому одно из важных требований, предъявляемых к конструкции устройств для ввода топлива в топку, - обеспечение интенсивного подсоса продуктов сгорания. Уменьшению времени нагрева и подсушки также способствует более высокая температура в топке. С этой целью при сжигании топлив с началом выхода летучих при высоких температурах (более 400 °С) в камерных топках делают зажигательные пояса, то есть закрывают экранные трубы огнеупорным теплоизоляционным материалом, чтобы снизить их тепловосприятие.
При сжигании топлива в слое роль каждого вида источников тепла определяется конструкцией топки. В топках с цепными решетками нагревание и подсушка осуществляются преимущественно лучистым теплом факела. В топках с неподвижной решеткой и подачей топлива сверху подогрев и подсушивание происходят за счет движущихся через слой снизу вверх продуктов сгорания.
В процессе нагревания при температуре выше 110 °С начинается термическое разложение органических веществ, входящих в состав топлив. Наименее прочными являются те соединения, которые содержат значительное количество кислорода. Эти соединения распадаются при сравнительно невысоких температурах с образованием летучих веществ и твердого остатка, состоящего преимущественно из углерода.
Молодые по химическому составу топлива, содержащие много кислорода, имеют низкую температуру начала выхода газообразных веществ и дают их больший процент. Топлива с малым содержанием соединений кислорода имеют небольшой выход летучих и более высокую температуру их воспламенения.
Содержание в твердом топливе молекул, которые легко подвергаются разложению при нагревании, оказывает влияние и на реакционную способность нелетучего остатка. Сначала разложение горючей массы происходит преимущественно на наружной поверхности топлива. По мере дальнейшего прогревания пирогенетические реакции начинают происходить и внутри частиц топлива, в них повышается давление и внешняя оболочка разрывается. При сжигании топлив с большим выходом летучих коксовый остаток становится пористым и имеет большую поверхность по сравнению с плотным твердым остатком.
2. Процесс горения газообразных соединений и кокса
Собственно горение топлива начинается с воспламенения летучих веществ. В период подготовки топлива происходят разветвленные цепные реакции окисления газообразных веществ, сначала эти реакции протекают с малыми скоростями. Выделяющееся тепло воспринимается поверхностями топки и частично накапливается в виде энергии движущихся молекул. Последнее приводит к возрастанию скорости цепных реакций. При определенной температуре реакции окисления идут с такой скоростью, что выделяющееся тепло полностью покрывает теплопоглощение. Эта температура является температурой воспламенения.
Температура воспламенения не является константой, она зависит как от свойств топлива, так и от условий в зоне воспламенения, в среднем составляет 400-600 °С. После воспламенения газообразной смеси дальнейшее самоускорение реакций окисления вызывает повышение температуры. Для поддержания горения необходим непрерывный подвод окислителя и горючих веществ.
Воспламенение газообразных веществ приводит к окутыванию коксовой частицы огневой оболочкой. Горение кокса начинается, когда к концу подходит горение летучих. Твердая частица прогревается до высокой температуры, и по мере уменьшения количества летучих веществ снижается толщина пограничного горящего слоя, кислород достигает раскаленной поверхности углерода.
Горение кокса начинается при температуре 1000 °С и является самым длительным процессом. Причина в том, что, во-первых, снижается концентрация кислорода, во-вторых, гетерогенные реакции протекают более медленно, чем гомогенные. В итоге длительность горения частицы твердого топлива определяется в основном временем горения коксового остатка (около 2/3 общего времени). Для топлив с большим выходом летучих, твердый остаток составляет менее ½ начальной массы частицы, поэтому их сжигание происходит быстро и возможность недожога невысока. Химически старые топлива имеют плотную частицу, горение которой занимает почти все время нахождения в топке.
Коксовый остаток большинства твердых топлив в основном, а для некоторых видов - целиком состоит из углерода. Горение твердого углерода происходит с образованием окиси углерода и углекислого газа.
Оптимальные условия для тепловыделения
Создание оптимальных условий для процесса горения углерода - основа правильного построения технологического метода сжигания твердых топлив в котельных агрегатах. На достижение наибольшего тепловыделения в топке могут оказывать влияние следующие факторы: температура, избыток воздуха, первичное и вторичное смесеобразование.
Температура. Тепловыделение при сжигании топлива существенно зависит от температурного режима топки. При относительно низких температурах в ядре факела имеет место неполнота сгорания горючих веществ, в продуктах сгорания остаются окись углерода, водород, углеводороды. При температурах от 1000 до 1800-2000 °С достижимо полное сгорание топлива.
Избыток воздуха. Удельное тепловыделение достигает максимального значения при полном сгорании и коэффициенте избытка воздуха, равном единице. С уменьшением коэффициента избытка воздуха выделение тепла падает, так как недостаток кислорода приводит к окислению меньшего количества топлива. Понижается температурный уровень, снижаются скорости реакций, что приводит к резкому уменьшению тепловыделения.
Повышение коэффициента избытка воздуха больше единицы снижает тепловыделение еще сильнее, чем недостаток воздуха. В реальных условиях сжигания топлива в топках котлов предельные значения тепловыделения не достигаются, так как присутствует неполнота сгорания. Она во многом зависит от того, как организованы процессы смесеобразования.
Процессы смесеобразования. В камерных топках первичное смесеобразование достигается подсушкой и перемешиванием топлива с воздухом, подачей в зону подготовки части воздуха (первичного), созданием широко раскрытого факела с широкой поверхностью и высокой турбулизацией, применением подогретого воздуха.
В слоевых топках задача первичного смесеобразования состоит в том, чтобы подавать необходимое количество воздуха в разные зоны горения на решетке.
С целью обеспечения догорания газообразных продуктов неполного горения и кокса организуют процессы вторичного смесеобразования. Этим процессам способствуют: подача вторичного воздуха с высокой скоростью, создание такой аэродинамики, при которой достигается равномерное заполнение факелом всей топки и, следовательно, вырастает время пребывания газов и коксовых частичек в топке.
3. Образование шлака
В процессе окисления горючей массы твердого топлива происходят значительные изменения и минеральных примесей. Легкоплавкие вещества и сплавы с низкой температурой плавления растворяют тугоплавкие соединения.
Обязательным условием нормальной работы котлоагрегатов является бесперебойный отвод продуктов сгорания и образующегося шлака.
При слоевом сжигании шлакообразование может приводить к механическому недожогу - минеральные примеси обволакивают недогоревшие частиц кокса либо вязкий шлак может перекрывать воздушные проходы, преграждая доступ кислорода к горящему коксу. Для снижения недожога применяют различные мероприятия - в топках с цепными решетками увеличивают время нахождения шлака на решетке, производят частую шуровку.
В слоевых топках вывод шлака производится в сухом виде. В камерных топках шлакоудаление может быть сухим и жидким. Таким образом, горение топлива является сложным физико-химическим процессом, на который оказывает воздействие большое количество различных факторов, но все они должны быть учтены при проектировании котлов и топочных устройств. www.wirbel-rus.ru Горение жидкого топлива | Cжигание твердого топливаЗдравствуйте! В зависимости от условий протекания процесса горения в реакцию может вступить большая или меньшая доля исходных веществ. Для полного использования химической энергии топлива необходимо реакции горения топлива доводить практически до конца. В условиях промышленного сжигания топлива равновесие реакций горения достигается редко ввиду малого количества времени протекания реакций горения. Процесс горения жидкого и твердого топлива в теории горения называют гетерогенным горением, поскольку он протекает в неоднородной (гетерогенной) системе. Если же горит смесь газов, то горение называют гомогенным. При горении жидкого топлива в топочной камере происходит испарение топлива с поверхности капель. Образующиеся пары топлива вследствие высокой температуры в топке подвергаются термическому разложению и быстро сгорают у поверхности частиц. В этих условиях скорость процесса горения определяется интенсивностью испарения топлива. С целью увеличения суммарной поверхности капель жидкое топливо при подаче в топочную камеру подвергается мелкодисперсному распыливанию с помощью форсунок (поверхность при этом возрастает в несколько тысяч раз). Неиспарившиеся из капельки тяжелые фракции подвергаются термическому разложению (крекингу), в результате чего образуется дисперсный углерод, придающий свечение пламени. Процесс горения твердого топлива можно разделить на две стадии. После испарения из топлива влаги происходит горение летучих веществ, которые выделяются в результате термического разложения топлива. Затем начинается горение твердого остатка (кокса). При очень быстром нагревании топлива обе стадии накладываются друг на друга, так как часть летучих веществ сгорает вместе с углеродом кокса. Кокс частично подвергается газификации, и образующиеся газообразные продукты, состоящие в основном из окиси углерода СО, сгорают в топочном пространстве. Горение твердой частицы топлива происходит не только с ее поверхности, но и в объеме вследствие проникновения кислорода в поры. При этом на поверхности частицы образуется пограничный (ламинарный) слой газа, в котором уменьшается содержание кислорода и увеличивается содержание продуктов газификации и горения (СО и СО2). Этот пограничный слой газа препятствует подводу кислорода, и скорость реакции горения будет зависеть от скорости диффузии окислителя через пограничный слой. Для увеличения интенсивности горения увеличивают скорость окислителя (воздуха) относительно поверхности частиц топлива, что уменьшает толщину пограничного слоя. На процесс горения топлива значительно влияют также минеральные примеси (зольность). По мере выгорания углерода на поверхности частиц топлива образуется слой золы. При низкой температуре размягчения золы и высоком содержании ее этот слой обволакивает (шлакует) частицы топлива и ухудшает процесс горения. Для удаления золового нароста при слоевом сжигании топлива производят шуровку, то есть рыхление слоя топлива. В мощных современных котлах твердое топливо сжигается во взвешенном состоянии. Куски топлива предварительно размалываются в специальных мельницах, что увеличивает их удельную поверхность в несколько сот раз. Смесь топливной пыли и воздуха подается в топочную камеру, где топливо воспламеняется и сгорает в газовоздушном потоке. Горение топлива также протекает в две стадии, однако время сгорания частицы топлива при этом значительно уменьшается. Такой способ сжигания позволяет интенсифицировать процесс горения, а также полностью механизировать все производственные операции. Исп. литература: 1) Хзмалян Д.М., Каган Я.А. Теория горения и топочные устройства, Москва, «Энергия», 1976; 2)Теплотехника, Бондарев В.А., Процкий А.Е., Гринкевич Р.Н. Минск, изд. 2-е,"Вышейшая школа", 1976. teplosniks.ru Особенности горения жидкого топливаКатегория: Отопительные системы Особенности горения жидкого топливаГорение — это химический процесс окисления горючих компонентов топлива, сопровождающийся интенсивным выделением теплоты.Известно, что при низких температурах наличие топлива и воздуха (окислителя) не обеспечивает их химического соединения, называемого горением. Горение начинается только после того, как частицы прогрелись до температуры, обеспечивающей им энергию активации Е, достаточную для вступления в реакцию. Частицы топлива и окислителя, обладающие начальным энергетическим уровнем Н, должны приобрести энергию активации. Для достижения энергетического уровня А, при котором реакция будет идти самопроизвольно, необходимо предварительно преодолеть энергетический барьер, равный разности энергетических уровней А и Н, после чего начинается экзотермическая реакция, идущая до точки К и сопровождающаяся выделением энергии (теплоты) в количестве ЕА_К. Предварительный подогрев, необходимый для зажигания топлива, первоначально создается внесением в топку горящего факела, искры или другого источника высокой температуры. В дальнейшем частицы горящего топлива, горячие газы, а также накаленные теплоизлучающие стенки топочной камеры способствуют подогреву и протеканию реакции горения вновь поступающей топливно-воздушной смеси. При нагреве жидкого топлива с недостатком воздуха происходит испарение углеводородов и их термическое разложение, сопровождающееся расщеплением углеводородов. В результате расщепления образуются легкие и тяжелые углеводороды. Легкие углеводороды и водород быстро сгорают при благоприятных условиях (достаточная температура, наличие кислорода). Тяжелые, высокомолекулярные углеводороды и сажистый углерод очень трудно сгорают, вследствие чего значительная несгоревшая их часть уносится из топки либо образует в топках коксовые наросты. Копоть и сажа в пламени также являются результатом образования тяжелых, высокомолекулярных углеводородов. Таким образом, процесс горения жидкого топлива проходит следующие стадии: смешение капель топлива с воздухом, подогрев их и испарение, термическое разложение (расщепление), образование газовой фазы, воспламенение и завершение оксидирования (горения) газовой фазы. Стадии эти неотделимы одна от другой и в какой-то мере совмещаются. Образовавшаяся после прохождения первых стадий горения газовая смесь легко воспламеняется и быстро сгорает. Если процесс нагрева и испарения частиц топлива протекает быстро, то при достаточном количестве кислорода создаются наиболее благоприятные условия для полного горения, в противном случае происходит глубокий распад углеводородов с образованием трудносжигаемых частиц. Мелкое распыление частиц топлива и равномерное их распределение увеличивают активную (поверхность реакции, облегчают нагрев и испарение частиц и способствуют процессу быстрого и полного горения. Разложение углеводородов идет симметрично при сравнительно низких температурах (до 600 °С). При более же высоких температурах распад молекул идет несимметрично: наряду с легкими углеводородами образуются тяжелые углеводородные комплексы, наиболее трудносжигаемые. При условии тонкого, равномерного распыления топлива и хорошего смешения его с воздухом, по возможности подогретым, подводе всего воздуха к корню факела создаются наилучшие условия горения жидкого топлива. Важно также, чтобы образование частиц тяжелых углеводородов и сажистого углерода, неизбежное в той или иной степени, происходило возможно раньше, чтобы частицы не уносились в атмосферу, а успевали полностью сгорать в зоне интенсивного горения. Таким образом, основные условия эффективного сжигания жидкого топлива сводятся к следующему: необходимо обеспечить подвод всего количества воздуха к устью факела, мелкое и равномерное распыление топлива, тщательное смешение частиц топлива и воздуха, турбулентность потока, подогрев воздуха, высокую температуру и хорошую воспламеняемость топлива в топке. Подвод воздуха в количествах, теоретически необходимых для горения топлива (стехиометрическая смесь), может обеспечить полное сгорание топлива лишь в случае очень тонкого его распыления и тщательного смешения с воздухом. Поэтому практически воздух подают в количестве, несколько большее, чем это необходимо для создания стехиометрической смеси. Однако во избежание чрезмерного охлаждения смеси избыток воздуха не должен быть слишком большим. При двойном количестве воздуха воспламенение и горение топлива чрезвычайно затрудняется и даже становится невозможным. Сгорание отдельной капли топлива можно представить следующим образом: в результате подогрева капля начинает испаряться, пары топлива, окружающие каплю, диффундируют в окружающую среду, происходит взаимопроникание частиц воздуха и топлива. При достаточной температуре смесь паров топлива к кислорода воздуха начинает активно реагировать, происходит процесс диффузионного сгорания газовой фазы топлива. Скорость химической реакции очень велика, скорость же физических процессов (испарение капли, смешение паров топлива с окислителем, подогрев смеси) значительно меньше, и очевидно эти физические процессы определяют скорость сгорания. В основном время сгорания зависит от времени испарения и времени диффузии молекул. Ламинарная диффузия определяет спокойный, сравнительно медленный процесс, турбулентная — ускоренный процесс. С уменьшением размера капель уменьшается время их испарения. Испаряемость топлива, его плотность, состав и условия теплообмена с окружающей средой также влияют на скорость горения. Горение жидкого топлива состоит из процессов его распыле-ния, смешения с воздухом (окислителем), испарения и реакции соединения с окислителем.Величина поверхности частиц топлива, омываемых воздухом и вступающих в реакцию с кислородом, имеет решающее значение для интенсивного и полного сгорания топлива. Величина активно реагирующей поверхности топлива определяется степенью и качеством его распыления, а также качеством смешения его с воздухом. Однородное и тонкое распыление топлива является обязательным и важным фактором подготовки топлива к сжиганию. Распыление топлива — процесс дробления струи на мелкие капли. Для распыления струи жидкого топлива необходимо преодолеть силы сцепления и поверхностного натяжения. Для создания развитой поверхности топливных струй применяются следующие методы: распыление топлива сжатым воздухом, паром или дутьевым воздухом от вентилятора; распыление топливной струи за счет действия центробежных сил в механических форсунках; создание тонкой конусовидной пленки вращающимся распылителем в ротационных форсунках; газификация топлива; распределение топлива тонкой пленкой на поверхностях корпуса горелки. Наиболее совершенное распыление достигается сжатым воздухом или паром, однако для этого требуется компрессор или паровой котел. При распылении топлива дутьевым воздухом также получается хорошее качество распыления, однако здесь необходим вентилятор высокого или среднего давления (не менее 3000—4000 Па). Недостатком метода распыления с помощью форсунок является наличие вращающихся механизмов с довольно сложной кинематической передачей в механических форсунках, а в ротационных — еще требуется топливный насос высокого давления, а также система фильтрации топлива. Все перечисленные способы распыления топлива применяются при расходах топлива не ниже 5—10 кг/ч, что существенно превышает потребность в топливе бытовых печей. По этим причинам для установки в бытовых отопительных и отопительно-варочных печах могут быть рекомендованы только методы газификации и распределения топлива тонкой пленкой в корпусе горелки. При этом требуется минимальное количество вспомогательного оборудования, причем расход топлива может быть минимальным. Для того чтобы обеспечить эффективное протекание процесса горения жидкого топлива, необходимо правильно проводить его теоретический расчет.При расчетах горения топлива требуется определять следующие величины: количество воздуха, теоретически необходимого для горения; количество образующихся продуктов сгорания; коэффициент избытка воздуха в продуктах сгорания; теоретическую температуру горения. Точный расчет этих величин производится по данным элементарного состава топлива на основе количественных соотношений реакций горения. Для различных марок жидкого топлива, имеющего достаточно стабильный элементарный состав, выведены упрощенные формулы для расчета процессов горения в следующем виде. Отопительные системы - Особенности горения жидкого топливаgardenweb.ru Процесс горения топлива]]>Горением называется взаимодействие горючих веществ с кислородом воздуха. Процесс горения может происходить только при высокой температуре и, как правило, сопровождается выделением определенного количества тепла. Если пламя свечи покрыть стаканом, то она начнет дымить и затем погаснет. Горение прекратится потому, что весь кислород воздуха в стакане израсходовался, а без кислорода горение происходить не может. Если кусок дерева поместить в сосуд с кислородом — он гореть не будет, так как сосуд не нагрет. Горючие части топлива— углерод и водород — могут соединяться с кислородом, только в сильно нагретом состоянии. Следовательно, без высокой температуры топлива горение происходить не может. Для воспламенения дерева, например, нужно, чтобы его температура была не ниже 300°, для каменного угля — 600°. Как происходит обычная растопка печи? Сложенные в печи дрова окружены кислородом, поступающим в виде потока воздуха через топочную и поддувальную дверцы. Однако даже сухие дрова нельзя зажечь одной спичкой, небольшое пламя которой не в состоянии сильно нагреть полена. Сначала спичкой зажигают растопку (мелкую лучину или бумагу), а от е& пламени нагреваются и загораются дрова. Чтобы горение происходило непрерывно, в печь все время должен поступать кислород (воздух). Если количество воздуха слишком велико, то топливник будет охлаждаться, а горение — ухудшаться, так как для хорошего горения необходима высокая температура. Поэтому нельзя топить печь с широко открытой дверцей. Если же количество воздуха, а следовательно, и кислорода недостаточно, то происходит так называемое неполное горение— дрова тлеют и горят темно-красным пламенем, выделяя большое количество густого черного дыма, в котором уносятся частички топлива, не сгоревшего из-за недостатка кислорода. В дымооборотах печи и в дымовой трубе эти частички осаждаются в виде сажи. Для того чтобы воздух проникал во всю толщу топливного слоя и обеспечивал кислородом всю поверхность горения, печи оборудуют колосниковыми решетками и поддувалами. Если поддувала нет и воздух попадает через топливную дверцу, то он омывает только передний ряд дров, поднимается кверху и уходит в дымоход, не соприкоснувшись с задними рядами дров. Поэтому дрова полностью не сгорают. Печи без поддувала и колосниковой решетки гораздо хуже используют сгорающее топливо. Внешними признаками полного сгорания топлива являются: соломенно-желтый цвет пламени в топливнике и белый или прозрачный дым. При полном сгорании сажа почти не откладывается на стенках дымооборотов и дымовой трубы. Нормальный процесс горения протекает при высоких температурах: для дров 800—900° и для каменного угля 900— 1200°. Эти температуры обеспечивают непрерывность горения, если кислород в топливники подается также непрерывно. При полном сгорании углерода 1 весовая часть его соединяется с 2 весовыми частями кислорода воздуха и дает в результате 1 весовую часть нового газа, называемого углекислым газом или углекислотой. Этот газ, не имеющий цвета и запаха, не горит и не поддерживает горение. При неполном сгорании углерода образуется окись углерода. Этот газ может гореть при высокой температуре. Окись углерода ядовита. Небольшое содержание ее в воздухе помещения может вызвать серьезное отравление и даже смерть людей; в быту окись углерода называют угаром. Внешним признаком выделения окиси углерода служат синенькие короткие огоньки поверх слоя углей. При сгорании водорода 2 весовые части его соединяются с 1 весовой частью кислорода, образуя водяной пар, который уносится в дымовую трубу. Если температура отходящих газов низка или стенки дымовой трубы сильно охлаждены, то и водяные пары охлаждаются и оседают на стенках в виде капель воды (иногда смешанной с несгоревшими частицами топлива). Это явление называется конденсацией водяных паров. Пии постоянной конденсации ухудшается тяга. Стенки трубы отсыревают и она постепенно разрушается. Из этого следует, что нельзя допускать чрезмерного остывания дымовых газов; температура их не должна быть ниже 125—150°. Дымовые газы представляют собой смесь продуктов сгорания топлива из углекислоты, окиси углерода, водяных паров, остатков несгоревших частиц топлива (сажи) и иногда паров серы. ikamin.ru Процесс - горение - топливоПроцесс - горение - топливоCтраница 2 Процессы горения топлива, запрессованного в смесь, и реакции образования клинкерных минералов протекают в обжигаемой смеси слитно. [16] Процесс горения топлива может быть полным и неполным. При неполном горении остается окись углерода - угарный газ. Происходит это вследствие недостатка кислорода ( воздуха), необходимого для полного процесса горения. [17] Процесс горения топлива может быть полным и неполным. [18] Процесс горения топлива в современных эмалеварочных печах осуществляется в рабочей камере печи, непосредственно над расплавом, поэтому топливо должно иметь возможно более высокую теплотворную способность и возможно меньшее содержание серы и золы. Этим требованиям в большей степени удовлетворяют газообразное и жидкое топлива, имеющие ряд преимуществ перед твердым топливом. [19] Процесс горения топлива зависит от ряда факторов, важнейшими из которых являются качество топлива ( химический состав, размерная характеристика), режим работы котла ( интенсивность горения, форсировка), метод отопления, конструкция топки, способ подвода воздуха и квалификация кочегара. [20] Процессы горения топлива в цилиндре ДВС рассматриваются как процессы подвода эквивалентного количества теплоты к рабочему телу. [21] Процесс горения топлива идет при постоянном давлении и непрерывном увеличении объема продуктов сгорания. [22] Процесс горения топлива представляет собой химический процесс соединения горючих элементов топлива с кислородом воздуха, протекающий при высокой температуре и сопровождающийся интенсивным выделением тепла. В результате процесса горения образуются газы, называемые продуктами сгорания или дымовыми газами, а также твердые остатки - зола, шлак и частицы несгоревшего топлива. [23] Процесс горения топлива условно можно разбить на несколько стадий. При горении твердого топлива можно выделить три стадии - воспламенение ( зажигание), активное горение и догорание. В первой стадии твердое топливо вначале подогревается, подсушивается и при температуре 105 - 110 С теряет свою влагу. При температуре около 150 - 180 С топливо начинает разлагаться на летучие вещества и твердый остаток - кокс. Этот процесс усиливается с повышением температуры и наиболее бурно протекает при температуре 300 - 400 С. [24] Процесс горения топлива на цепной решетке отличается от процесса горения на неподвижной решетке, когда свежее топливо забрасывается на горящий слой и горение его начинается снизу. В топках с цепными решетками топливо поступает на холодную часть решетки и, получая теплоту излучения факела и стенок, загорается сверху. [26] Процесс горения топлива в печах регулируется подачей воздуха на горение в каждую горелку по величине и цвету факела. Процесс горения топлива контролируется автоматическими газоанализаторами по содержанию окиси углерода и кислорода в дымовых газах. [27] Процессы горения топлив в потоке под давлением, в том числе в присутствии ряда сред, имеют самостоятельное значение для решения некоторых энергетических и главным образом технологических задач, поэтому они также отражены в монографии. Процессы при высоких температурах приобретают несколько иной характер, так как в этих условиях протекают и качественно и количественно иные химические реакции с образованием таких соединений, которые не могут получаться при обычных температурах. Технико-экономическая целесообразность таких процессов обусловливается не только получением химических соединений, но и энергетическим использованием теплового потенциала высокотемпературных процессов. [28] Процесс горения топлива в такого рода малогабаритных топках следует организовать так, чтобы зона горения топлива была наименьшей, а полнота сгорания наибольшей, во всяком случае не хуже, чем в котельных топках. [29] Процессы горения топлив в присутствии некоторых сред имеют самостоятельное и не менее важное значение, чем процессы горения с участием различных сред. К этой категории относятся, например, процессы, протекающие в камерах сгорания газовых и парогазовых турбин. Как известно, в камерах сгорания ГТУ процесс горения топлив организован в присутствии больших избытков воздуха ( в 3 - 4 раза выше стехиометрического расхода), который в этих условиях становится нейтральной теплопогло-щающей средой. [30] Страницы: 1 2 3 4 www.ngpedia.ru |
|
||||||||||||||||||
|
|
||||||||||||||||||
|




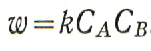 (1)
(1)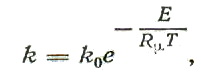 (2)
(2)





